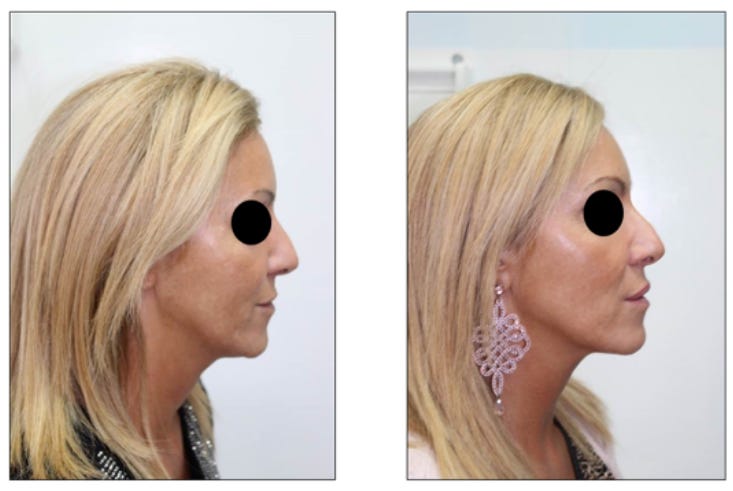
Na minha opinião sincera, este é de longe o melhor e mais completo TCC para obtenção do título de Especialista em Harmonização Orofacial no assunto Toxina Botulínica que você vai ler. Aqui você encontra a transcrição do Trabalho de Conclusão de Curso apresentado ao Instituto Velasco, pela Dra. Patricia Martins Costa.
O tratamento com toxina botulínica moderna foi iniciado por Alan B. Scott e Edward J. Schantz no início da década de 1970, aprovado pela FDA em 1989 quando o sorotipo A foi utilizado na medicina para corrigir o estrabismo. Em 1989, o BoNT-A (onabotulinumtoxin-A), foi inicialmente aprovado para o tratamento de estrabismo e blefarospasmo pela Food and Drug Administration dos EUA (FDA).
A seguir, Toxina Botulínica tipo A (BTX-A) começou a ser utilizada pelos neurologistas como tratamento para doenças neuromusculares tais como distonias e espasticidades sendo a mesma liberada pela FDA em 2002 para o tratamento de rugas faciais.4
A característica que torna a Toxina Botulínica tipo-A útil para esses várias condições é a inibição da liberação de acetilcolina na junção neuromuscular. 1
Como a técnica de aplicação da BTX-A não gera efeitos colaterais sistemicos, o estudo para seu uso tem se desenvolvido, surgindo várias novas indicações.
Embora novos usos da Toxina Botulínica tipos A e B (BTX-A e BTX-B) continuem sendo estudados em condições neuromusculares (tiques, tremor, gagueira, marcas causadas pela acne, dores musculares cronicas) que envolvem o sistema nervoso somático, também se reconheceu que os efeitos desses medicamentos não estão confinados a neurônios colinérgicos na junção neuromuscular.2,3 Receptores para BTX-A e O BTX-B também são encontrados nos terminais nervosos autonômicos, onde inibem a liberação de acetilcolina. Esta observação levou a estudos com a Toxina Botulínica em várias condições que envolvem a inervação autonômica como distúrbios híper-secretores (hiperidroses), rosácea, psoríase, doenças de pele raras como Fox-fordyce, Hailey-Hailey, dermatose bolhosa e pachyonichia congenita.
Os receptores BoNT-A e os alvos intra-celulares não são exclusivos para a neurotransmissão. Eles foram encontrados em células neuronais e não neuronais, mas existem diferenças na forma como o BoNT-A se liga e atua sobre células neuronais e não neuronais.
As células não neuronais que expressam uma ou mais proteínas de ligação a BoNT-A e ou a proteina Snap-25 associada ao sinaptossoma alvo da clivagem, inclui: queratinócitos epidérmicos; células estaminais mesenquimais do tecido adiposo subcutâneo; células da mucosa nasal; células uroteliais; células epiteliais intestinais, da próstata e alveolares; linhas de células da mama; neutrófilos; e macrófagos. O sorotipo BoNT-A também pode provocar efeitos biológicos específicos efeitos em fibroblastos dérmicos, sebócitos e células endoteliais vasculares.
A down-regulation da reação inflamatória também tem sido usada para o controle de diversos quadros como melhoria do processo cicatricial e da aparência de cicatrizes e queloides7. Como amplamente conhecida, a pele interage com o sistema nervoso e há evidências crescentes de que o sistema neurológico participa diretamente da inflamação cutânea e da cicatrização de feridas1,2. A Toxina Botulina leva a supressão da atividade dos mastócitos .
Já no controle da dor cronica como a fibromialgia, dores neuropáticas continuas e intermitentes, dores na ATM cronicas não remissíveis com os tratamentos convencinais enxaquecas cronicas, dor devido a artrite reumatoide e esclerose múltipla, a Toxina Botulinica trabalhará no Sistema Nervoso inibindo a sensibilização do mesmo, tanto a nível periférico como a nível central através de vários mecanismos como a inibição de substância P, do peptídeo relacionado ao gene da calcitonina (CGRP), do receptor vanilóide transitório 1 (TRPV1) e a liberação de glutamato.3
A Toxina Botulinica também aparece com inovações em seu uso hiperdiluido (microbotox) assim como em associação com o Acido Hialurônico nas chamadas terapias combinadas.7
A base do tratamento com BoNT-A para a acne e pele oleosa, proporcionando redução na produção de sebo, parece estar na ação da acetilcolina nos receptores muscarinicos das glândulas sebáceas. Esses receptores controlam a diferenciação do sebócito e produção de sebo . 42
O controle da oleosidade da pele também se dá pela paralisação dos tono- filamentos que se encontram em torno do folículo piloso, levando a atrofia das glândulas sebáceas.7
Foi documentado que a BoNT - A inibe o crescimento de células cancerígenas da próstata humana LNCaP in vitro e in vivo 78 e também aumenta a forma fosforilada da fosfolipase-A2, o que pode representar um mecanismo que explica como o toxina reduz o crescimento e a proliferação celular. 71
Para o desenvolvimento deste trabalho foram utilizadas pesquisas de artigos indexados na Pub-med e Scielo e livros técnicos .
NEUROTRANSMISSORES, NEUROMODULAÇÃO E DOWN-REGULATION
Para um maior entendimento da ação da BTX-A, é preciso ter em mente o que são os neurotransmissores, a neuromodulação e a down-regulation .
NEUROTRANSMISSORES
São os neuroquímicos que são liberados pelos neurônios pré-sinápticos na fenda sináptica e ativam canais iônicos, são chamados de neurotransmissores. Eles são liberados tanto a nível de SNP como a nível de SNC.
Os Neurotransmissores podem ser de duas classes: moléculas pequenas, sendo de ação rápida, ou moléculas grandes, que são moléculas caracteristicamente de ação lenta.6
As moléculas pequenas, de ação rápida são aquelas que em sua maioria causam respostas agudas no sistema nervoso, como respostas sensórias dentro e para o SNC e sinais descendentes motores para os músculos.6
As moléculas grandes são os neuropeptídios e representam um grupo diferente de substâncias químicas. Eles não são fabricadas no terminal pré-sináptico, mas nos ribossomas do corpo neuronal e depois são transportadas para as sinapses e liberadas na fenda sináptica.
Sua ação é lenta, mas ,quando liberados, possuem ação muito mais longa nos neurônios pós- sinápticos.6
Há evidências crescentes de que a inervação cutânea é capaz de modular uma variedade de fenômenos cutâneos agudos e crônicos, interagindo com as células da pele e seus componentes imunes. Essa forma de sinalização local entre tecido nervoso e tecido cutâneo ocorre especialmente por meio dos neuropeptídeos, uma numerosa família de neurotransmissores de natureza química comum e nomenclatura heterogênea presentes em todo o sistema nervoso e secretados pelas fibras nervosas cutâneas.
NEUROTRANSMISSORES DE AÇÃO RÁPIDA
As pesquisas atuais revelam a neuromodulação da BTX-A sobre os seguintes neurotransmissores de ação rápida:
ACETILCONINA (ACH)
É o neurotransmissor mais comum encontrado nos seres humanos. É secretada por vários neurônios em muitas áreas do cérebro, mais especificamente no córtex motor, gânglios da base, e neurônios motores que inervam os músculos esqueléticos6.
Em quase todas as situações, a acetilcolina tem um efeito excitatório pós - sináptico. Ela também é considerada um neurotransmissor que possui intensa ação vasodilatadora.
GLUTAMATO
É um aminoácido secretado nos terminais pré-sinapticos em muitas vias sensitivas, assim como em muitas áreas do córtex cerebral.
Seu efeito será sempre excitatório.
NEUROTRANSMISSORES DE AÇÃO LENTA
SUBSTANCIA P
É um neurotransmissor neuropeptídeo, composto por uma cadeia de 11 resíduos de aminoácidos que atua como neuromodulador. A substância P facilita processos inflamatórios, vômito, ansiedade e nocicepção (resposta a dor). Pode ser encontrado tanto no sistema nervoso central quanto no periférico.
A SP é secretada pelos nervos sensitivos específicos e células com função inflamatória como macrófagos, eosinófilos, linfócitos e células dendríticas e atua ligando-se ao receptor da neuroquinina-1 (NK-1R).
CGRP (peptídeo relacionado ao gene da calcitonina).
O CGRP pode ser produzido em neurônios periféricos ou centrais. É um potente vasodilatador peptídico e pode atuar na transmissão da nocicepção (envio de sinais de dor ao cérebro). Na medula espinhal, a função e a expressão do CGRP podem diferir dependendo de onde ele é sintetizado. O CGRP produzido por neurônios motores no corno anterior da medula espinhal pode contribuir para a regeneração do tecido nervoso após a lesão. Por outro lado, CGRP derivado do gânglio da raiz dorsal no corno dorsal da medula espinhal pode estar ligado à transmissão da dor. No sistema vascular do trigêmeo, os corpos celulares no gânglio trigêmeo são a principal fonte de CGRP. Acredita-se que o CGRP desempenhe um papel na homeostase cardiovascular e na nocicepção.7
O CGRP estimula, ainda, a proliferação de células endoteliais8,9 e de melanócitos in vitro.9 Como anti-inflamatório, entretanto, o CGRP é capaz de inibir muitas funções das células de Langerhans.
METALOPROTEINASES
As metaloproteinases, também chamadas de matrixinas, são endopeptidases dependentes do Zinco. Promovem a degradação da matriz extra-celular (de macromoléculas). No geral, a maioria das metaloproteinases de matriz se relaciona à enzima colagenase, incluindo MMP-1, MMP-8, MMP-13 e MMP-18. Porém, as metaloproteinases podem ser subdivididas em 4 categorias, de acordo com a sua preferência em um determinado substrato: colagenase (MMP-1, -8, -13 e-18); gelatinase (MMP-2 e -9); estromelisina (MMP-3 e -10) e metaloproteinases tipo de membrana (MMP-14, -15, -16 e -17).
As fibras elásticas são facilmente decompostas pela secreção e ativação das elastases através da exposição à radiação UV ou ROS (espécies reativas de oxigênio).
CITOCINAS
Citocinas são polipeptídeos ou glicoproteínas produzidas por diversos tipos celulares e capazes de modular a resposta celular de diversas células, incluindo dela própria. São moléculas hidrossolúveis e de tamanho variado. Podem ser divididas no grupos: interleucinas (IL), fatores estimuladores de colônias (CSF), fator de necrose tumoral (TNF), interferons (IFN) e fatores de crescimento (TGF).
Estão relacionadas a respostas imunes, regulando sua duração e intensidade. Recrutam células efetoras como Monócitos, macrófagos e linfócitos
Instituto Velasco - instituto.velasco@gmail.com - IP: 189.120.72.103
NEUROMODULAÇÃO
Neuromodulação é uma tecnologia que atua diretamente sobre os nervos. É a alteração - ou modulação - da atividade nervosa, fornecendo agentes elétricos ou farmacêuticos diretamente a uma área-alvo.
Logo, o uso da BTX-A implica na neuromodulação controlada. Seja no intuito de controle da dor, do processo inflamatório, inibição de substância P, peptídeo relacionado ao gene da calcitonina (CGRP) e liberação de glutamato.3
DOWN-REGULATION
A down-regulation ou regulação negativa é a diminuição na expressão celular de um receptor específico em resposta ao aumento da ativação por uma molécula, como um hormônio ou neurotransmissor, que reduz a sensibilidade da célula à molécula. Este é um exemplo de mecanismo de ação local (feedback negativo).
Com relação a ação da BTX-A seu efeito será de down-regulation (parcial) ou de bloqueio neuromuscular pré-sináptico (total) nas junções neuromusculares.
CICATRIZAÇAO DE FERIDAS
A cicatrização de feridas é um processo complexo e dinâmico que é dependente das atividades coordenadas de múltiplos tipos de célula no epitélio, tecido conjuntivo e vascular. 10
Além disto, o processo é imperfeito causando muitas vezes desfigurações e alteraçoes na qualidade da cicatriz, ela sofre a influencia da região da lesão sendo processo inflamatorio prolongado. Pode haver atraso na epitelização e sofre a influencia da tensão causada por músculos adjacentes perpendicular a lesão que pode estar gerando: 101,12,14
Microtraumas;
Exarcebação da reação inflamatória;
Superprodução de colágeno e glicosaminoglicanos;
Reparação tecidual com com atraso;
Hiper-pigmentação da cicatriz;
Três fases da cicatrização
FASE INFLAMATÓRIA (OU MIGRATÓRIA)
Duração de alguns dias;
Citocinas e fatores de crescimento presentes;
Celulas inflamatorias macrófagos, neutrófilos e fibroblastos;
FASE PROLIFERATIVA (OU MITÓTICA)
Dura semanas
Formação de tecido de granulação. Os fibroblastos produzem a matriz
extracelular (MEC), para fechamento da ferida e crescimento vascular.
Miofibroblastos ajudam a iniciar a contração da ferida.
FASE FINAL (MATURAÇÃO)
Ferida é fechada e normalmente dura por 7 meses;
Cicatriz começa a diminuir;
Diminuição do edema;
Diminuição de células inflamatórias;
A MEC é degradada;
Angiogênese e fibroplasia;
Colágeno tipo III imaturo é substituido pelo colágeno maduro tipo I;
CICATRIZ HIPERTRÓFICA E QUELOIDE
Existe uma diferença de classificação em cicatrizes hipertróficas e queloides.
CICATRIZ HIPERTRÓFICA
Cicatrizes elevadas que permanecem dentro dos limites originais da ferida são conhecidos como cicatriz hipertrófica.
QUELÓIDE
Quando o tecido cicatricial se expande além dos limites da ferida original como um resultado da atividade contínua de fibroblastos, a cicatriz é passa a se chamar quelóide. 15
Cicatrizes hipertróficas e quelóides faciais são desfigurantes e são frequentemente associados a sintomas clínicos como prurido, dor , amplitude restrita de movimento
e contratura. 11
FISIOPATOLOGIA DA CICATRIZ HIPERTRÓFICA E QUELOIDE
Quelóides e cicatrizes hipertróficas são condições fibróticas da pele caracterizada por hiperproliferação de fibroblastos e excesso de deposição de colágeno.
Quelóides e cicatrizes hipertróficas estão associados com atividade desregulada da metaloproteinase (MMP). Estudos recentes indicam que a atividade da MMP-2 pode estar patologicamente aumentada em quelóides e cicatrizes hipertróficas, levando a uma produção elevada de colágeno.
A patogênese da cicatriz quelóide e hipertrófica ocorre devido disfunção na granulação da ferida, causada pelo fator de crescimento transformador hiperativo-b (TGF-b) e atividade da Proteinas Smad disfuncionais. 26,27 O TGF-b fator de crescimento transformador hiperativo-b (TGF-b) que regulam a produção de colágeno em nível transcricional. 31,32
A cicatrização de feridas é freqüentemente um processo imperfeito que deixa manchas, cicatrizes e possível desfiguração. Isso pode ser influenciado pela localização da ferida, inflamação prolongada, infecções de feridas e atraso na epitelização (mais de 10 dias) .11,12,13.
Os músculos da expressão facial, assim como os músculos mastigatórios alteram a tensão na pele adjacente. Se esta tensão é exercida perpendicularmente a ferida durante o processo de cicatrização, pode haver a geração de micro-traumas em curso para a lesão, o que exacerba inflamação, levando à superprodução de colágeno e glicosaminoglicanos e atraso na cicatrização. 11,12,14
Isso resulta na formação de cicatrizes elevadas e muitas vezes hiperpigmentadas, que freqüentemente estão em posições de destaque no rosto. 10
MECANISMO DE AÇÃO DA BTX-A NAS CICATRIZES HIPERTRÓFICAS E QUELÓIDES
A injeção de BoNT-A pode melhorar significativamente a aparência cosmética das cicatrizes faciais. 11
O mecanismo molecular do BTX em cicatrizes hipertróficas e quelóides ainda não está perfeitamente explicado, mas o BTX demonstrou inibir a proliferação de fibroblastos derivados de cicatrizes hipertróficas tecidos. Além disso, é relatado que o BTX suprime a expressão do fator de crescimento transformador (TGF-b) , colágeno I e III, - actina muscular lisa e proteína miosina II em fibroblastos de queloides. 29,30
O TGF-b promove quimiotaxia de fibroblastos e medeia a expressão de Proteínas Smad, que regulam a produção de colágeno em nível transcricional. 31,32
O BoNT-A diminuiu o TGF-b e atividade Smad-2 em fibroblastos derivados de modelos de contratura de cicatriz . 33,34
Miofibroblastos disfuncionais contribuem para a formação de cicatrizes quelóides e hipertróficas. 90 A inibição da proliferação de fibroblastos, leva a uma diminuição da produção da citocina inflamatória e do fator de crescimento transformador (TGF) - β1 - principal regulador da hipertrofia na formação de cicatrizes 18 e do fator de crescimento do tecido conjuntivo; 13,16
No geral, o BoNT-A parece modular a deposição de colágeno, mas ainda não está claro como a expressão dos genes de colágeno e MMP é regulada. 20
Um aspecto particularmente favorável do BTX é sua capacidade de controlar os sintomas subjetivos da cicatrizes hipertróficas. O BTX pode imobilizar os músculos locais de uma cicatriz e reduzir a tensão da pele causada pela tração muscular e. Isso alivia as fibras nervosas presas nos quelóides, neutralizando a coceira e a dor associado à neuropatia de fibras pequenas.
Tem sido muito utilizada na região mentoniana, abdominal, asa do nariz (em alectomias) e reparos de cicatrizes mal formadas. O BoNT-A pode ser usado para reduzir ou suavizar cicatrizes problemáticas, particularmente aqueles em áreas com extensa atividade muscular, como a testa superior e queixo. Se uma cicatriz não se conforma naturalmente, então o BoNT-A foi usado para aliviar a tensão criada pela atividade muscular sob a cicatriz.
Outra vantagem do BTX é a ausência de atrofia da pele e telangiectasia, geralmente observada após injeção de esteroides.
A BTX-A pode aumentar a expressão do fator de crescimento endotelial vascular (VEGF) aumentando assim, a angiogenese , embora os mecanismos precisos subjacentes à formação de cicatriz hipertrófica e quelóides não estejam totalmente compreendidos; 15
PROTOCOLOS DE APLICAÇÃO
DOSE: A injeção de BoNT-A pode variar de 10 a 40 UI .
LOCAL DE APLICAÇÃO - A BoNT-A pode ser empregada tanto no local da formação de cicatrizes como no local da remoção da sutura.19
RUBOR FACIAL / ERITEMA/ ROSÁSEA
RUBOR FACIAL E ERITEMA
O rubor facial consiste em um episódio de vermelhidão associado com uma sensação de queimação. Pode ser primário ou idiopático e secundário a rosácea ou a estímulos hormonais como os da menopausa. Foi provado que o BoNT-A fornece alívio sintomático em pacientes com rubor facial através da inibição da via de sinalização da acetilcolina.
MECANISMO DE AÇÃO DA BTX-A NO RUBOR FACIAL E NO ERITEMA
Um possível mecanismo pelo qual o BTX-A melhora a descarga é o potente bloqueio da acetilcolina liberada dos nervos periféricos autonômicos do sistema vasodilatador cutâneo3,4 . O outro mecanismo envolvido, é a inibição da liberação de mediadores inflamatórios, como a substância P e o peptídeo relacionado ao gene da calcitonina (CGRP) 5 . A redução e o controle da inflamação local da pele podem permitir a eritema a desaparecer.
ROSÁCEA
É uma doença crônica que atinge, principalmente, mulheres entre 30 e 50 anos. Ela não é contagiosa e tem origem desconhecida. A rosácea aparece como área avermelhada, com pápulas e pústulas que se manifestam no rosto e podem comprometer os olhos e o nariz. 40
A rosácea tem uma apresentação variável. Às vezes, o diagnóstico clínico da rosácea pode ser difícil de identificar, mas seu sinal mais importante é o eritema na face central, que persiste por mais de três meses. Rubor, pápulas, pústulas e teleangiectasias são outros sinais característicos comuns. 37
CLASSIFICAÇÃO DA ROSÁCEA
A rosácea pode ser classificada em quatro subtipos:
ERITEMATO-TELANGIECTÁTICA
A rosásea eritematotelangiectática, a pele fica muito vermelha e repleta de vasos (telangectasias). Isso é muito evidente principalmente na região centro facial. O avermelhamento pode ser agravado por vários fatores, entre eles: o álcool, sol, estresse, exercícios físicos e calor. Quem possui a rosácea, tem a sensação de estar com a pele pinicando ou queimando. Neste caso, a pessoa afetada é sensível a qualquer creme. 40
PAPULOPUSTULAR
A rosácea papulopustular (PPR) é a rosácea clássica caracterizada por uma porção central vermelha da face com pequenas pápulas que podem ser superadas por pústulas pontuais. A descarga ocorre, mas não é tão marcada quanto na ETR. Inflamação persistente ou episódica é comumente vista, e a inflamação pode levar a edema crônico e alterações fibrosas da pele.
FIMATOSA
A rosácea fimatosa (phymatous) é caracterizada pelo espessamento acentuado da pele e nodularidades irregulares da superfície, levando a rinofima (nariz), gnathophyma (queixo) e metophyma (testa). É caracterizada pelo aumento e infiltração de áreas como as glândulas sebáceas do nariz e é comum em homens com mais de 40 anos. Com o tempo, o nariz pode até dobrar de tamanho. 40
OCULAR
O quarto tipo, rosácea ocular, gira em torno dos olhos. Cerca de 20% dos casos são descobertos em visita a um oftalmologista. O indicativo da doença é uma inflamação (chamada de blefarite) com avermelhamento e descamação na área dos cílios. Este tipo é o mais grave de todos, podendo evoluir para a perda da visão. 40
Outras considerações clínicas para a rosácea incluem rosácea glandular granulomatosa representada por nodularidades que podem levar a cicatrizes, mas não estão necessariamente associadas ao rubor.
Condições não-rosáceas, como danos crônicos ao sol, abuso tópico de esteróides e reações adversas a medicamentos, podem ter sintomas semelhantes aos da rosácea e devem ser descartadas antes do diagnóstico da rosácea.
MECANISMO DE AÇÃO DA BTX-A NA ROSÁCEA
Os resultados de estudos36 sugerem que o mecanismo da Toxina botulínica no tratamento da rosácea envolve o bloqueio da degranulação de mastócitos pela inativação do complexo SNARE dentro da célula. 36 Portanto, o BoNT-A não apenas visa o componente inflamatório neurogênico da rosácea, mas também tem efeitos inibitórios diretos nos mastócitos. Esses vários alvos do BoNT-A podem oferecer vantagens terapêuticas sobre as medicações atualmente disponíveis.
PROTOCOLOS DE TRATAMENTO NA ROSÁCEA
A BoNT-A foi investigado em vários estudos de caso de pacientes com rosácea recalcitrante. A média de doses usada foi de 25U (variando entre 15-45 U).
Injeções intradérmicas de BoNT-A na glabela e / ou bochechas em intervalos de 0,5 cm. Pacientes relataram uma melhora nos sintomas dentro de 2 semanas tratamento e os efeitos duraram até 4 meses. 38
2 sessões de tratamento com BoNT-A intradérmica em intervalos de 1 semana. A dose total BoNT-A foi de 50 unidades nas 2 sessões. Os efeitos duraram 3 meses. 38,39
ACNE E PELE OLEOSA
A acne é uma condição inflamatória da pele que ocorre quando folículos pilosos (regiões em que nascem os pelos) ficam obstruídos por sebo e células mortas, gerando espinhas, cravos, cistos, caroços e cicatrizes.
Existem vários fatores que atuam no desenvolvimento da acne na pele. Entre eles, o aumento do sebo da pele ou da oleosidade da mesma gerada por mudanças na glândulas sebáceas se torna um fator de alta relevância. 42
Apesar da glândula sebácea não ser inervada pela sistema nervoso parassimpático, foi recentemente provado que a sinalização da acetilcolina influencia diretamente a produção dos lipídios. 41
A oleosidade excessiva na pele oleosa pode ser causada por: lavagem excessiva da região, utilização de produtos contra-indicados para esse tipo de pele, limpeza da pele com as mãos sujas, uso de água quente para lavar o rosto, falta de hidratação, alimentos com alto índice glicêmico, desequilíbrio hormonal e exposição ao sol sem proteção.
MECANISMOS DE AÇÃO DA BTX-A NA ACNE E PELE OLEOSA
A base do tratamento com BoNT-A para a acne e pele oleosa, proporcionando redução na produção de sebo, parece estar na ação da acetilcolina nos receptores muscarinicos das glândulas sebáceas. Esses receptores controlam a diferenciação do sebócito e produção de sebo . 42 Os receptores colinérgicos são expressos em sebócitos humanos e a acetilcolina induziu síntese lipídica em sebócitos humanos. 41
A pele oleosa pode ser mais suscetível à regulação colinérgica do que a pele normal devido à maior abundância de sebócitos e assim, com a presença de mais receptores colinérgicos.41
O controle da oleosidade da pele também se dá pela paralisação dos tono- filamentos que se encontram em torno do folículo piloso, levando a atrofia das glândulas sebáceas.7
PROTOCOLO DE TRATAMENTO DA BTX-A NA ACNE E PELE OLEOSA
Injeções intra-dermicas de BoNT-A nas regiões afetadas com intervalos de 0,5 cm.
SUGESTÃO DE PROTOCOLO SEGUNDO CALVANI E COLS. 43
INDICAÇÕES
A intenção é diminuir a atividade do suor e das glândulas sebáceas para melhorar a textura e o brilho da pele e atingir a camada do SMAS onde os músculos que encontram inseridos à superfície inferior da derme, causando ritides visíveis.
Tratamento de face e pescoço pela injeção da toxina botulínica na derme ou no plano sub-dérmico para melhorar a textura da pele, suavizar vincos horizontais e diminuir as bandas verticais do pescoço, bem como para obter uma melhor aposição do platisma ao maxilar e pescoço, melhorando o contorno do ângulo cervico- mentual.
TÉCNICA DE INJEÇÃO SUPERFICIAL DE BONT-A
Realizada através da injeção dérmica de micro-doses de toxina botulínica, não por seringa tradicional, mas com técnica de agulhamento que consiste em várias micro- gotas distribuídas por dispositivo elétrico (dermapen).
A solução da toxina botulinica é hiperconcentrada quando comparada à diluição tradicional ou comparada ao microbotox ou mesobotox. ( tabela 1).
Além disso, a técnica de injeção é diferente porque a dispersão de micropartículas superficiais não é realizada, mas quantidades pequenas, homogêneas e controladas de solução são gotejadas ao mesmo tempo que o Dermapen faz as perfurações. Cada seringa de 0,8 ml contém 50 unidades de onabotulinumtoxin-A.
A solução é entregue por via intradérmica, o Dermapen utilizado foi ajustado com uma cabeça de 24 agulhas profundidade de 3,0 mm estendida para 3,5 mm.
A área do rosto a ser tratada é separada do pescoço e mandíbula, e uma grade é criada com base no tamanho do diâmetro da cabeça de o instrumento utilizado (Figura 1).

A técnica envolve tratar, em uma sessão, as áreas selecionadas e dividido como mencionado anteriormente, deixando cair uma gota de suspensão botulínica (0,1 ml) sobre a pele e colocar imediatamente Dermapen firmemente acima do líquido no mesmo local por 3 segundos medidos por uma cronometria digital (Figura 2).

São aplicadas cerca de 3000 perfurações por área, (o dispositivo realiza cerca de 60.000 perfurações / min).
Para aumentar a duração do tempo de tratamento, o protocolo foi padronizado com 3 sessões por 3 meses. A primeira sessão com a técnica descrita, enquanto os 2 últimos com a mesma técnica sem administrar toxinas, mas apenas com o trauma do agulhamento no tecido.
As duas técnicas conjugadas desempenham uma ação dupla na pele. Observou-se que o micro-trauma induz a produção fatores de crescimento por multiplicação de fibroblastos e a síntese de colágeno e elastina.
CONTROLE DA DOR
EFEITOS PERIFÉRICOS
A ação da BoNT-A além de bloquear a liberação de Ach, também inibe a liberação de neuropeptídeos nociceptivos locais (particularidade da TBX-A), como a substância P, CGRP e o glutamato, assim como a expressão potencial do Receptor Transitório Vanilóide 1 (TRPV1). 44,45.
O TRPV1 é um receptor ionotrópico que intensifica a excitabilidade dos nociceptores, respondendo a estímulos nocivos, como calor e substâncias pró- analgésicas. 49
A BoNT - A inibe a translocação do TRPV1 mediada pela proteína SNARE para a membrana plasmática49. O TRPV1 tem um papel importante durante o processamento da dor térmica e inflamatória periférica.
As SNAREs são proteínas que basicamente que desempenham um papel central na geração da especificidade do tráfego vesicular e na catálise do processo de fusão da vesícula á membrana plasmática. As SNAREs intervêm na exocitose das vesículas de transporte celular, que entram em contato com a membrana celular ou com os lisossomas. Muitas vesículas transportadoras só se formam se um tipo específico de proteína Rab e SNARE estiverem acopladas à sua membrana, permitindo assim que a vesícula se funda corretamente.
Supõe-se que a inibição da sensibilização periférica leve a uma inibição indireta da sensibilização central e, portanto, seja um mecanismo possível para a eficácia do BoNT-A na dor crônica.
EFEITOS CENTRAIS
Recentemente, o foco das pesquisas dos efeitos anti-nociceptivos da BoNT-A tem sido na pesquisa da existência efeitos centrais da Toxina Botulínica, particularmente através do transporte axonal retrógrado dos nervos sensoriais e motores. 59
Estudos demonstram efeitos bilaterais da BoNT-A após injeção unilateral da toxina, indicando potencial etiologia central 51. Estudos adicionais demonstram a detecção do SNAP-25 clivada pela BoNT- A no corno dorsal do núcleo caudal trigêmeo após injeção periférica de BoNT-A e nos cornos dorsal e ventral ipsi-laterais da medula espinhal de ratos após a injeção de BoNT-A no nervo ciático de ratos 51,52,53 e nos astrócitos espinhais após a injeção periférica do nervo ciático 53.
A relação entre o os efeitos anti-inflamatórios e anti-nociceptivos do BoNT - A ainda são controversos. 51
RECOMBINAÇÃO GENICA
Pesquisas da recombinação genica de tipos diferentes de Toxina Botulinica tem sido realizadas no intuído de aumentar o potencial terapêutico da mesma .
Os tipos estudados tem sido a BoNT-A e a BoNT-E. Clivando o SNAP-25 em diferentes locais, o BoNT-A e o BoNT-E têm durações de ação muito diferentes58 Ao passo que os efeitos paralisadores da musculatura da BoNT- A duram meses em humanos e semanas em ratos; a BoNT - E atua por períodos curtos de dias.
A BoNT- A reduz a taxa de fusão, a BoNT- E inibe completamente a fusão da vesícula, semelhante aos efeitos do VAMP. 60
A BoNT- E pode entrar no neurônio cultivado mais rápido que a BoNT – A, com maior potência, podendo assim, inibir a transmissão na junção neuromuscular mais rapidamente. Ela também não é afetada pelo aumento do Ca++ no citosol celular. Essas propriedades do BoNT - E são atraentes para melhorar versões terapêuticas da BoNT; no entanto, o BoNT - E também tem uma desvantagem - pode produzir fraqueza muscular transitória - em comparação com a longa duração da ação de BoNT- A.
Para encontrar um domínio responsável pelas propriedades, a metade C-terminal da cadeia pesada foi trocada para criar quimeras.
No estudo de Wang et al. 55, as quimeras foram produzidas trocando a metade C-terminal da cadeia pesada nos domínios entre BoNT- A e E58 . O EA recombinante possui a cadeia leve e metade N-terminal dos domínios da cadeia pesada de BoNT- E e a metade C-terminal da cadeia pesada de BoNT- A, enquanto AE compreende a cadeia leve e a metade N-terminal da cadeia pesada de BoNT-A.
A troca de domínios da BoNT produz novos recursos; a quimera EA foi de ação rápida e mais potente que o BoNT - A na junção neuromuscular. E a quimera EA era tão potente e rápida quanto o BoNT - E, e eles eram equivalentemente sensíveis a inibição dependente da dose da bomba de prótons vesicular. AE produziu fraqueza muscular persistente, o que pode ser um efeito potencialmente terapêutico para o uso no futuro.
CONTROLE DA DOR NA ODONTOLOGIA
Na odontologia poderemos tratar cefaleias crônicas primarias com componentes musculares, dores miofasciais, enxaquecas primarias e dores neuropáticas contínuas e episódicas48,51 com o uso da BoNT – A.
Tem sido pesquisado o uso da BoNT – A intra-articular em casos de dor intra- articular refratários. 83
Faz-se imperativo que o profissional saiba realizar o diagnóstico diferencial entre os vários tipos de dor de cabeça para que o tratamento adequado quanto a dose, pontos de aplicação e co-morbidades sejam controlados nestes casos.
O diagnóstico diferencial para caracterização das dores crânio faciais é bastante complexo e inclui doenças cujas origens primárias podem não se encontrarem localizadas na face. Daí a necessidade de um diagnóstico minucioso que deve ser realizado através da história clínica da doença, exames complementares e clínicos bastante elaborados. 61
A localização, os fatores de melhora e piora, o caráter, o modo de apresentação assim como os sinais e sintomas associados a cefaléia são de grande valia.
Os resultados dos exames complementares como por exemplo, tomografia computadorizada, radiografias e ressonância magnética, assim como avaliações odontológicas oftalmológicas, otorrinolaringológicas, e quando necessário a execução de bloqueio anestésicos diagnósticos, devem ser analisados com bastante cuidado. 61
TOXINA BOTULINICA E A DOR MUSCULAR
Acreditava-se que a BoNT-A reduzia a dor apenas ao induzir relaxamento muscular, inibindo a liberação de acetilcolina; este fato pode reduzir indiretamente a isquemia dolorosa que pode ser causada por um músculo híper-contraido. No entanto, houve alguns casos em que o alívio da dor foi observado mesmo em pacientes que não apresentaram melhora na contração muscular hiperativa. Também foi descoberto que o alívio da dor existia mesmo depois que os efeitos do relaxamento muscular desapareciam, medido pela força de mordida reduzida em pacientes tratados por desordens temporomandibulares54 .
Doses mais baixas (50 unidades) foram necessárias para induzir efeitos analgésicos, enquanto doses mais altas (100 a 150 unidades) foram necessárias para criar um efeito de diminuição na contração muscular.
Isso implica, como já citado anteriormente, que a ação da BoNT-A além de bloquear a liberação de Ach, também inibe liberação de neuropeptídeos nociceptivos locais, como a substância P, o CGRP e o glutamato, assim como a expressão do potencial do receptor vanilóide transitório 1 (TRPV1). 44,45
TOXINA BOTULINA INTRA-ARTICULAR (ATM)
Os estudos para a redução de dores intra-articulares teve inicio em 2007, realizados em ratos. Estes estudos comprovaram a eficácia da redução da dor intra-articular da BoNT-A em função de sua ação anti-nociceptiva, gerada pela inibição de liberação de neurotransmissores dos neurônios sensoriais primários. 83 Os mesmos levaram os pesquisadores a ensaios de injeções intra-articulares para o tratamento de dor nas articulações em seres humanos.
A justificativa de tal uso se faz para os casos de dor intra-articular refratários (dor após um ano de tratamento completo (exceto cirúrgico). O tratamento das DTMs é complexo e inclui o uso de analgésicos, relaxantes musculares e anti-inflamatórios, anti-depressivos tricíclicos, fisioterapia (massagem, abertura da boca exercícios, mobilizações mandibulares, reposicionamento da língua, correção postural), e placas oclusais e as vezes tratamento psicológico. Além disto, o uso da injeção intramuscular do BoNT-A para relaxar os músculos e visco-suplementação realizada através das injeções intra-articulares de hialuronato de sódio devem ser realizadas antes que se parta para um protocolo de uso da BoNT-A intra-articular.
PROTOCOLO DE TRATAMENTO DA BTX-A NA DOR DA ATM
O protocolo utilizado nos estudos que foi efetivo revelou que o uso em media de 30U de BoNT-A, intra-articular, realizada com agulhas de 23G. 82
O relato foi da diminuição da dor em 66 % dos pacientes com a diminuição de até 2 pontos na EVA ( escala visual análoga).
Mais uma vez foi demonstrado que a BoNT-A interfere na síntese de neurotransmissores e neuro-moduladores polipeptídeos como Substância P e CGRP, que são mediadores-chave da inflamação neurogênica. 84,85 A BoNT-A também inibe citocinas, e outros mediadores inflamatórios, reduz a liberação de neuropeptídeos e em ambos modelos de dor neuropática e dor não neuropática. 86\
DESCOBERTA DE NOVOS SITIOS DE ACÃO DA TOXINA BOTULÍNICA
TOXINA BOTULÍNICA E AS CÉLULAS NÃO NEURONAIS
Existem várias células não neuronais que sofrem a ação direta da Toxina Botulínica, tanto na pele humana quanto em outros tecidos. Para tal, as células necessitam de expressar as seguintes proteínas de ligação, que estarão se ligando a BoNT– A61.
Proteína SV2 - que é uma proteína vesicular. A BoNT– A pode inibir a SV2 que se expressa em linhas celulares de câncer de mama. 62
Proteína FGFR3- receptor do fator de crescimento de fibroblastos;
Receptores Vanilóides;
SNAP-25;
SNAP-23,11,19,20, que estão expressas em tecidos humanos. 63
As células que possuem tais receptores acima alencados são:
Queratinócitos epidérmicos; 64,65
Células-tronco mesenquimais;
Tecido adiposo sub-cutâneo; 66
Células da mucosa nasal; 67
Células uroteliais; 68
Células epiteliais intestinais; 68,69
Células epiteliais da próstata; 71
Células epiteliais alveolares; 72
Linhas de células da mama; 62
Neutrófilos63 e macrófagos. 74
Além disso, a BoNT- A pode modular a ação dos fibroblastos dérmicos, mastócitos, sebócitos e células dos vasos endoteliais. 61
DIFERENÇAS NA LIGAÇÃO DA NEUROTOXINA BOTULÍNICA A NEURONIO E CÉLULAS NÃO NEURONAIS
DIFERENTES VIAS DE ENTRADA
As vias neuronais são dependentes da clarina;
Vias não neurais fazem usos de outros caminhos, como por exemplo as vias
intestinais que são dependentes de uma via da Cdc 42; 69
O HA, um dos componentes não tóxicos da cadeia pesada da toxina botulínica, interrompe a função de barreira inter-celular mediada pela
caderina-E facilitando a absorção para-celular de BoNT-A e BoNT -B 75 afetando a morfologia e viabilidade celular de uma maneira dependente do gangliosídeo GM3; 76
Na BoNT– C, a HA interrompe a função de barreira afetando a morfologia e viabilidade celular de uma maneira dependente de gangliosídeo GM3; 76
DIFERENÇAS NA AÇÃO DA TOXINA BOTULÍNICA NOS NEURÔNIOS E CÉLULAS NÃO NEURONAIS
A BoNT - A exibe efeitos diferenciais na expressão gênica em células neuronais e não neuronais. Estas diferenças podem se expressar aumentando ou diminuindo gens.
A análise por microarray (tecnologia combina a imuno-preciptação da cromatina com micro-arranjo de DNA e é utilizada para analisar as interações entre proteínas e DNA in vivo) da expressão genérica alterações na exposição ao BoNT - A revelaram que, em células humanas de carcinoma do cólon HT-29, 167 genes foram aumentados enquanto 60 genes foram desregulados, enquanto Células de neuroblastoma SH-SY5Y, cerca de 223 genes foram aumentados e 18 genes foram desregulados. 77
O perfil transcricional global da linha celular de macrófagos alveolares murinos (Murino é o modelo animal). Macrófagos murinos são derivados destes modelos, geralmente camundongos e ramsters) RAW 264. 64 revelou que genes alterados estavam envolvidos principalmente em sinais transdução, imunidade e defesa, modificação de metabolismo de proteínas , atividades neuronais, tráfico intracelular de proteínas e contração muscular.
EFEITOS CUTÂNEOS DA AÇÃO DA NEUROTOXINA BOTULÍNICA
SOBRE A VASCULATURA CUTÂNEA
Aumento da perfusão sanguínea - aumento do diâmetro do lúmen, diâmetro arterial externo e relação lúmen / espessura da parede; 11
No nível molecular, BoNT - A afetou a expressão do fator de crescimento;
Endotelial vascular, molécula de adesão celular endotelial plaquetária 1,
CD31, CD34, interleucina (IL) -1 . 11
POTENCIAL ANTI-PHOTOAGING
O potencial anti- fotoaging da BoNT– A pode ser constatado através da redução de proteínas relacionadas a senescência. Estudos com a irradiação da luz ultra-violeta em tecidos comprovou que após a aplicação da BoNT – A , houve nos fibroblastos a diminuição na expressão de b-galactosidase associada à senescência, aumento dos níveis de proteínas supressoras de tumor e associadas à senescência, proporção de células da fase G1 e diminuição da secreção de metaloproteinases da matriz MMP-1 e MMP-3, havendo também um aumento na produção de colágeno tipos I e III. 18 Carruthers e Carruthers sugerem que o efeito da BoNT-A na rede pré-sináptica e no sistema vascular (isto é, através da inibição da liberação neuropeptídeos vasodilatadores) e outros sistemas podem explicar o efeito aumentado dos sinais de envelhecimento - como linhas finas, rugas, telangiectasia e eritema - visto com BoNT-A e IPL. 100
A BoNT-A pode resultar em aumento organização da rede dérmica de colágeno e isso , juntamente com o aumento da produção de pro-colágeno, colágeno, e elastina, assim ela efetivamente reverte a perda de elasticidade e volume causado pelo envelhecimento. A síntese de colágeno pode ser aumentada simplesmente agulhando-se a pele, mas Permatasari e cols. confirmaram que o BoNT-A promove a síntese de colágeno e inibe a secreção de MMPs. 101
PROPRIEDADES ANTI- TUMORAIS
Os efeitos anti-tumorais da BoNT - A foram identificados em três tipos de linha celular de cancro, isto é, carcinoma da próstata, mama e cólon. 61 Foi documentado que a BoNT- A inibe o crescimento de células cancerígenas da próstata humana LNCaP in vitro e in vivo 78 e também aumenta a forma fosforilada da fosfolipase A2, o que pode representar um mecanismo que explica como o toxina aumenta a forma fosforilada da fosfolipase A2. 71 ( Na ausência de regulação estrita da atividade do PLA-2, é produzida uma quantidade desproporcional de mediadores pró- inflamatórios).
Em ratos, na infecção intra-prostática, a injeção BoNT - A alterou a dinâmica celular ao induzir apoptose, inibindo a proliferação e regulando negativamente receptores a1-adrenérgicos, associados à próstata, apoptose e alteração atrófica. 79,80 Os ratos tratados com toxinas mostrou coloração epitelial reduzida de Bcl-xL e consistentemente aumento da coloração de Bax e caspase-3 quando comparado com animais tratados com solução salina. 81 Como as linhas celulares da mama e do cólon demonstraram responder a BoNT-A por alterações na expressão gênica no RNA, outros tipos de câncer podem se tornar um potencial alvo para a atividade anti- câncer da BoNT-A.
TRATAMENTOS COMBINADOS
O envelhecimento facial é um processo tridimensional e os procedimentos de rejuvenescimento facial que visam reverter os efeitos do envelhecimento precisam resolver isso combinando produtos que relaxem a musculatura hipercinética, volumizem, preencham e contornem fazendo também, um efeito liffting na face. 87 Algumas áreas precisam ser preenchidas enquanto outras precisam ser levantadas. O rosto não envelhece como uma única massa contínua; mudanças abruptas de contorno e cisalhamento entre compartimentos adjacentes indicam que o envelhecimento facial é um processo tridimensional (3-D). 87
Como existem diferentes causas subjacentes do aparecimento das rugas, como a perda de volume ou atividade muscular hipercinética, são necessárias camadas de diferentes produtos para tratar todos os fatores contribuintes. A lógica por trás disto é semelhante à da construção de uma casa. Inibição da contração muscular primeiro fornece uma estabilidade base (fundação) para no segundo estágio, usando um preenchedor viscoso para melhorar a estrutura (alvenaria). Finalmente, os toques finais são aplicados com preenchedores de baixa viscosidade (acabamento). Este tipo de abordagem também ajuda a satisfazer as necessidades do paciente. 87
Os métodos de rejuvenescimento facial estão se tornando cada vez mais sofisticados. Hoje, combinações personalizadas de BoNT-A para corrigir rugas dinâmicas, cargas (como ácido hialurônico, hidroxilapatita de cálcio e ácido poli-l- láctico) , substâncias autólogas como tecido adiposo, para aumento de volume, lasers ablativos, tratamentos estimuladores de colágeno (como plasma rico em plaquetas , microneedling , radiofrequência e ultrassom) e descamação da pele para reverter a flacidez , podem obter resultados melhores que um tratamento individual, potencialmente em menor tempo, e com custo e inconveniência consideravelmente mais baixos para o paciente. Esse tipo de tratamento facial também resulta em satisfação do paciente muito alta (> 90%) . 89-94
O foto-envelhecimento reduz a produção de colágeno nos fibroblastos e, ao mesmo tempo, aumenta a secreção de metaloproteinases da matriz (MMPs), que decompõem o colágeno existente levando à perda de volume e elasticidade.
A BoNT-A pode resultar no aumento da organização da rede dérmica de colágeno, aumento da produção de pro-colágeno, colágeno e elastina - reverte efetivamente a perda de elasticidade e sua diminuição causada pelo envelhecimento.
Permatasari e cols. 100 confirmaram que o BoNT-A promove a síntese de colágeno e inibe a secreção de MMPs ( metaloproteinases da matriz) sendo uma grande aliada aos procedimentos estéticos de tratamento de pele.
TOXINA BOTULINICA E ACIDO HIALURONICO
TOXINA BOTULINICA E ACIDO HIALURONICO RETICULADO
Vários estudos indicam que uma combinação de BoNT-A e preenchimentos dérmicos podem alcançar maior durabilidade.89,92,95 Uma das justificativas para este fato, é que a maior duração dos preenchedores reticulados leva a um retorno gradual e de maior duração ao estado inicial do que o uso isolado da toxina botulinica. Somado a este fato, podemos citar o relaxamento da musculatura como sendo um facilitador ao preenchimento com Ácido Hialurônico.
SUGESTÃO DE PROTOCOLO
Pavicic and cols. 87 Sugerem o seguinte protocolo que foi realizado em sua pesquiza clinica:
Tratamento em 3 etapas sendo a primeira com BoNT-A , full face. E dois atendimentos separados posteriores a toxina onde foram utilizados, na segunda hidroxilapatita de cálcio e na terceira um ácido hialurônico monofásico - Filler.
Os resultados sugerem que essa abordagem de camadas com base no entendimento das causas subjacentes do envelhecimento facial, onde diferentes produtos são usados em combinação para tratar todo o rosto, pode permitir que os pacientes atinjam o resultado desejado de um retorno às características de um rosto mais jovem. No rejuvenescimento facial, envolvendo relaxamento muscular, espera- se que o volume alcançado com o preenchimento e o recontorno da face levando consequentemente à um liffting de toda a face sejam mais eficazes. 87
TOXINA BOTULINICA E ACIDO HIALURONICO NÃO RETICULADO
Os resultados para pacientes tratados com BoNT-A e o Acido hialuronico indicam que a dose correta é crítica, doses baixas não atingem o efeito desejado e algumas pacientes ficaram com características "congeladas" devido a overdose.
Este é um tratamento desafiador, devido à superficialidade e comprimento das linhas.
INDICAÇÕES
Pacientes com envelhecimento foto-ativo e perda de volume;
Linhas de arcodeon ou cara arranhada que se alongam da região orbital até
as têmporas e o pescoço;
Hipertrofia dos orbiculares e zigomáticos são os principais responsáveis por
rugas peri-orbitais e para-comissurais, mas rugas também podem aparecer a alguma distância esses músculos;
SUGESTÃO DE PROTOCOLO
O autor102,103 recomenda um máximo de 40 unidades de BoNT-A por lado. O tratamento bem-sucedido não apenas corrigiu a aparência arranhada do rosto, mas também melhorou sorriso e a aparência e textura da pele. 102,103 Os efeitos duraram de 4 a 6 meses. O uso de micro-cânulas diminui consideravelmente as perfurações na pele, se comparada ao uso de agulhas.
Os autores presentes encontraram o Aquagold Fine Dispositivo de micro- agulhamento de toque (Aquavit Pharmaceuticals, New York, NY), que também pode ser usado para fornecer combinações BoNT-A e preenchedores, para serem eficazes.
TOXINA BOTULINICA E ACIDO HIALURONICO NO PHOTOAGING
Regimes de tratamento projetados para rejuvenescer a pele podem melhorar os efeitos da BoNT-A usada sozinha. Estes regimes freqüentemente contêm retinóides e ou AH, cremes e soros. Os géis contendo o AH podem melhorar a hidratação e elasticidade da pele. 104
Pacientes que sofreram foto-envelhecimento substancial e perda de volume podem desenvolver conjuntos de finas linhas paralelas, que também podem ser profundas, estendendo-se da região orbital até as têmporas e o pescoço - uma condição variada descrita como “cara arranhada” ou “linhas de acordeão”. 105,106
A hipertrofia dos músculos orbiculares da boca e zigomáticos são responsáveis por rugas peri-orbitais e para-comissurais, mas as rugas também podem aparecer a alguma distância esses músculos. O tratamento é desafiador, devido à superficialidade e comprimento das linhas.
SUGESTÃO DE PROTOCOLO
A técnica desenvolvida por Môle et al. emprega injeções superficiais de substâncias altamente diluídas BoNT-A e HA não reticulado. 106 Enquanto os efeitos da toxina nos músculos é esperada, os efeitos nas áreas das bochechas são excelentes.
Os efeitos podem ser explicados pela difusão da toxina nas células dérmicas (facilitada diluição alta), onde o BoNT-A pode alterar as taxas de biossíntese de colágeno e produção de substâncias inflamatórias citocinas. 105
Os resultados para pacientes tratados com BoNT-A e Acido Hialuronico indicam que a dose correta é crítica, doses baixas não atingem o efeito desejado e pacientes onde houve uma overdose apresentaram características "congeladas" .
O investigador recomenda um máximo de 40 unidades de BoNT-A por lado. O tratamento bem-sucedido não apenas corrigiu a aparência arranhada do rosto, mas também melhorou sorriso ”e a aparência e textura da pele. 105,106
MICROBOTOX
Um método de aplicação chamado de "microbotox" foi desenvolvido por Wu em 2000, visando fornecer efeitos de aparência mais natural para os pacientes. 97
O método envolve a injeção sistemática de múltiplas pápulas de BoNT-A altamente diluído (principalmente ONA) em intervalos de 0,8 a 1,0 cm na derme ou na interface entre a derme e a superfície dos músculos faciais. Propõe-se que as micro-injecções suavizem as marcas da pele, induzam a atrofia em massa do suor glândulas sebáceas e enfraqueçam a superfície das fibras musculares que se inserem na pele (SMAS), reduzindo assim as linhas finas e rugas faciais.
A BoNT-A diluída impede a difusão nos músculos mais profundos, o que muitas vezes leva a uma aparência "congelada"95 A diminuição do suor e sebo pela diminuição da atividade da glândula melhora a aparência (qualidade) da pele especialmente na testa. 97
Há difusão da toxina nas células dérmicas (facilitada pela diluição alta), onde o BoNT-A pode alterar as taxas de biossíntese de colágeno e produção de substâncias inflamatórias/ citocinas.
Os efeitos do tratamento geralmente duram de 3 a 4 meses, mas podem durar até 6 meses.
SUGESTÃO DE DILUIÇÃO SEGUNDO OLIVEIRA
A diluição da TB para microdoses se inicia com a diluiçãode um frasco de 100U de toxina botulínicacom 2ml de soro fisiológico 0,9%. Dessa solução, retira-se 0,04ml (duas unidades) acrescentando-se 0,40ml (volume correspondente a 10 “unidades”) de soro fisiológico 0,9% em seringa BD Ultra Fine II® curta de 1ml e agulha 8mm, completando volume total de 0,48ml (12 “unidades”). Essa é a diluição final, sendo cada 0,04ml - 01 unidade.
MICROBOTOX E MICRO ÁCIDO- HIALURONICO RETICULADO
Kim, J.S descreve o uso de microdoses de acido hialuronico com microbotox misturadas. 98
Para a reconstituição do material de injeção, Microbotox e micro-acido- Hialuronico Reticulado polidensificada (Belotero Balance; Anteis, Genebra, Suíça, e distribuído pela Merz Pharmaceuticals) foi misturado com 1 ml (40 U) de toxina BoNT-A (Xeomin, Merz Pharmaceuticals, Alemanha) e 1 ml de solução salina normal. Essa mistura de Belotero e Xeomin foi denominada solução “XeoBel hydrotoxin” e pode ser usada em uma única sessão para Microbotox e Microhyaluronicacid.
Neste procedimento, 3 ml de a mistura XeoBel foi injetada em 990 locais no rosto. Portanto, a quantidade de toxina foi de aproximadamente 0,04 U, e a quantidade de S-HA foi de 0,001 ml por local de injeção. O injetor automático (injetor XeoBel; Contac-Korea, Seoul, Coreia) foi usado para injetar a solução na derme.
O injetor garantiu que a profundidade intradérmica fosse de 1,0 mm para todos os pacientes. A profundidade do injetor foi fixado em 1 mm e a profundidade real da injeção foi de aproximadamente 0,8 mm devido a chanfro na ponta da agulha. Este dispositivo possui nove agulhas de calibre 32, distribuídas de maneira que proporcionou uma distância regular (3,5 mm) entre as injeções.
Alterações da perda de água trans-epidérmica e hidratação do estrato córneo foram estatisticamente significantes às 4 e 8 semanas.
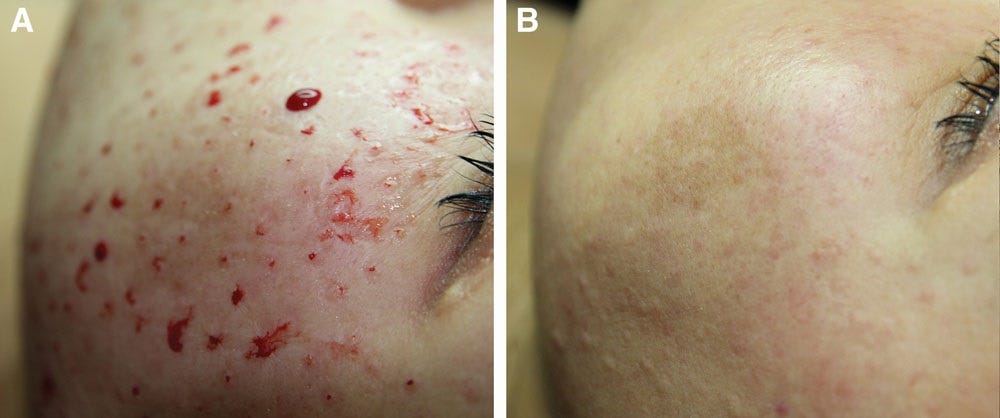
TOXINA BOTULINICA E LASER
O recapeamento a laser é usado para tratar epiderme e a superfície dérmica através da ablação epidérmica, levando a neo-colagênese, remodelação dérmica, e regeneração de organelas celulares. 93 99
Um pequeno ECR de face dividida demonstrou significativamente maior melhoria nas linhas de pés de galinha com ONA de 2 a 6 semanas antes do tratamento com um laser Erbium: YAG em comparação apenas com tratamento a laser. 107
O tratamento com BoNT-A demonstrou ter uma complementaridade e possivelmente efeito sinérgico, quando administrado após luz intensa pulsada (LPI) com fluência de 24 a 28 J / cm2.108
Embora o tratamento combinado dar excelentes resultados o custo do mesmo é elevado e deve ser levado em consideração. 110
TOXINA BOTULINICA E RETINÓIDES
O uso de retinóides tópicos diários, invertem o foto-envelhecimento impedindo destruição da matriz dérmica e promoção do colágeno. 94 Já o uso de cremes, soros e géis contendo o AH podem melhorar a hidratação e elasticidade da pele. 109 Outros componentes de regimes de tratamento de pele usados em combinação com a BoNT-A incluem hidroquinona para clareamento da pele, e adenosina, que foi proposto para agir por um número de mecanismos para reduzir rugas e melhorar o tom e textura da pele. 111
As injeções isoladas da BoNT-A demonstraram ter um efeito benéfico no volume e profundidade médios das linhas faciais, já o uso conjugado com os retinóides apresentou resultados melhores na híper-pigmentação , suavidade da pele e uniformidade do tom e cor da pele em comparação com o uso de injeções da BoNT-A isoladamente. 89, 94
Os produtos para a pele testados contendo adenosina, retinol e ácido hialurônico provaram ser um complemento útil à injeção de BoNT-A. 112
Firmeza, suavidade, tez, brilho e até cor e homogeneidade da pele, todos contribuem para a qualidade da pele, que também contribui para a percepção visual da idade.112 Como a qualidade pele é uma questão de cuidados diários, os praticantes precisam de produtos para a pele mais adequados ao procedimento escolhido: produtos com alta tolerância e possivelmente com benefício adicional.
NOVAS FORMULAÇÕES DA TOXINA BOTULÍNICA
TOXINA BOTULÍNICA TÓPICA
BoNT-A, daxibotulinumtoxin-A (RT001), estava sendo desenvolvida como um gel tópico para o tratamento de hiperidrose e pés de galinha. 121
A BoNT-A apresenta grande tamanho molecular, havendo assim, níveis insignificantes biodisponibilidade cutânea o que mostrou que aplicar soluções toxina na pele intacta não é eficaz. 121
ESTUDOS REALIZADOS
Dois estudos foram utilizados com a aplicação do Laser ablativo fracionário de penetração da derme. A penetração foi calibrada para não mais de 50 mm para evitar cicatrizes associado a aplicação de BTX-A 100U.
A intenção foi a de criar colunas na epiderme e derme com a expectativa que isso permitiria que moléculas de ABO atingissem orbicular inferior dos olhos e a derme superficial; 122,123
Embora o tratamento combinado tenha apresentado sucesso, os investigadores apontam que o procedimento é mais complicado e mais caro do que injeções.
Outro estudo foi realizado pela Revance, Newark, CA . Nesta formulação, o BoNT-A é complexado com um novo medicamento à base um sistema de entrega de peptídeos (Trans MTS; Revance, Newark, CA). Ao variar o comprimento dos peptídeos transportadores, a toxina pode ser entregue em uma profundidade definida ou site de destino.
ESTUDO FASE 1
Após 4 semanas, 89% dos pacientes no grupo ativo apresentaram uma redução clinicamente significativa na gravidade rugas em comparação com a linha de base (investigador e avaliação do paciente), com 44% atendendo às principais desfecho de eficácia de uma melhoria de ≥2 pontos; 120
ESTUDO FASE 2
Os resultados da fase III REALIZE 1 controlada por placebo estudo em 450 pacientes com pés de galinha moderados a graves (NCT02580370) demonstrou que não houve o delivery da droga nos sítios desejados, ou seja, não se atingiu os pontos finais primários ou outros.
Em vista dos resultados desfavoráveis, a Revance Therapeutics, Inc. (Newark, CA) divulgaram que não planejam continuar o desenvolvimento da RT001 tópica para pés de galinha, ou seguir o atual plano de desenvolvimento clínico para RT001 na hiperidrose axilar. 113
PEPTIDEO BOTULÍNICO TÓPICO E INTRA-DÉRMICO ASSOCIADO A ATIVOS
A marca suiça Meiskin Swiss lançou recentemente no mercado o BoLCA , uma linha de dermo-cosméticos que faz uso da nano-tecnologia TPC - Nanotechnology of Cellular Penetration + Peptideo botulinico (50 Kda), para uso tópico. 114,115
Quem faz uso da toxina botulínica injetável pode também usar este blend, de modo a complementar o tratamento anti-envelhecimento e prolongar consideravelmente o efeito da toxina botulinica injetável, com uma rotina diária e contínua. 114
O grande desafio à utilização tópica da toxina botulínica está associado ao seu alto peso molecular (Onabotulinumtoxin-A 900kD; Abobotulinumtoxin-A 500kD e Incobotulinumtoxin-A 150kD) que impede sua permeação pela camada córnea, epiderme viável e posteriormente derme. 115
A Meiskin Swiss adquiriu a patente e o direito de distribuição Mundial, do Ativo desenvolvido pela empresa de inovação tecnológica BPMed (Coréia) de nome técnico ATGC-BoLC, que é o ativo Nano Botulinum. 115
NANOTECNOLOGIA DE CARREAMENTO NANO-TPC
A tecnologia que foi utilizada em estudos anteriores era chamada de PTD (Protein Transduction Domain) cuja proposta é a penetração do ativo por endocitose. Para tal, grandes concentrações do ativo, assim como um longo tempo de contato do produto era necessário, fato que inviabilizou o uso desta tecnologia.
A proposta do BoLCA é o de possuir uma estrutura com capacidade de permeação atingindo células da derme com o uso tópico dos ativos. 115
Segundo os trabalhos apresentados pelo fabricante, 115 a eficácia da tecnologia Nano-TPC em carrear moléculas para o meio intracelular é viável. Logo, o mesmo torna-se capaz de carrear o peptídeo botulínico para dentro de melanócitos, queratinócitos e fibroblastos.
Segundo outro trabalho apresentado pelo fabricante, um estudo realizado em pele de cadáveres, avaliou a permeação do Fator de Crescimento estudado (GF) com e sem a nanotecnologia Nano-TPC.
Os resultados mostraram que a tecnologia de nanocarreamento aumentou em 30 vezes a capacidade de permeação do ativo. 115
O desenvolvimento de um peptídeo botulínico, contendo somente a cadeia leve da toxina botulínica, foi outra grande inovação tecnológica do ativo ATGC-BoLC.
A cadeia leve da toxina botulínica foi produzida por terapia recombinante, e recebeu a denominação técnica de Lc. A combinação da tecnologia Nano-TPC com a cadeia leve da toxina botulínica por terapia recombinante (Lc) foi denominada cientificamente de ATGC-BoLc e comercialmente Nano Botulinum.
Outro estudo apresentado pelo fabricante115 demonstra não haverem efeitos colaterais com o uso do ativo como citotoxidade (viabilidade celular), genotoxicidade (aberração cromossomica), mutagenicidade (mutação reversa) e testes clinicos para avaliação do potencial de irritabilidade e sensibilização dérmica foram realizados, porém não houve relatos dos resultados dos mesmos na bibliografia apresentada pelo fabricante115.
Da mesma forma támbém não foram apresentadas as questões relativas á um possível efeito vacina causado pelo produto, uma vez que o protocolo de aplicação profissional do mesmo é realizado através da técnica lançada por Wu e colaboradores em 2002 para a aplicação do Microbotox, onde o uso no microagulhamento é realizado a profundidade de 0,5mm como meio de se conseguir fazer o delivery do blend.
Entretanto, o protocolo requer a repetição desta apicação por 3 meses seguidos, somados ao uso tópico do blend home-care, para uso diário, que também possui o peptídio botulínico em sua fórmula na concentração de 0,5 partes por milhão (ppm) - Nano Botulinum (ATGC-BoLC -Peptídeo botulínico em nanocarreador Nano-PTC).
EFEITOS
Segundo o fabricante, o produto foi efetivo na redução da melhora da elasticidade em 14,82% e da recuperação da pele (firmeza) em 9,26%.
Um último teste clínico de eficácia avaliou, com parâmetros dermatológicos, a redução da profundidade do sulco nasogeniano obtendo escore de 17,65%. 115
Os ativos atuam na epiderme, derme, estimulando queratinocitos, fibroblastos e aumentando a produção de colágeno. A ideia do produto é melhorar a hidratação, iluminação e a revitalização da pele. Ele não promove o relaxamento muscular.
MÁSCARA FACIAL CALMANTE APÓS O TRATAMENTO
O uso da máscara pode ser associado ao uso do Sérum e do produto Profissional Dermoline Meiskin Swiss.
Para a ativação desses componentes são necessários apenas 20 minutos de contato, mas, para potencializar os resultados e tratar manchas e melasmas, o recomendado é permanecer com o produto de 30 a 40 minutos.
Para melhores resultados, utilize por 5 dias consecutivos, após esse período use 2 vezes por semana, para manutenção dos resultados. Retirar a máscara e enxaguar o rosto com água fria; 115
HOME CARE
Os cuidados são mantidos pelo paciente no home-care com o Sérum Facial Meiskin Swiss possui um blendde ingredientes, que auxilia na redução das rugas existentes, linhas de expressão, e prevenindo o aparecimento de novas. 114,115
Nano Botulinum (ATGC-BoLC -Peptídeo botulínico em nanocarreador Nano-PTC) a 0,5 partes por milhão (ppm). 115
Ação dérmica do peptídeo botulínico, estimulando a neocolagênese e a produção endógena de ácido hialurônico e outros elementos da Matriz extracelular. 115
TOXINA BOTULÍNICA FORMULAÇÃO LIQUIDA PRONTA
Uma formulação líquida estéril pronta para usar de um novo BoNT-A, MT10109L, desenvolvido por MedyTox, Inc. (Cheongju, Coréia do Sul), não requer diluição antes use e não contém albumina ou proteínas de origem animal. 117 O peso molecular e a capacidade de difusão do MT10109L são relatados como similares aos da ONA. Porém um estudo para comparar MT10109L com ONA no tratamento das linhas glabelares, demonstrou que houve diferenças de eficácia explicada pelo fato de que as unidades de potência dos produtos botulínicos são específicos para cada família de produtos e não são intercambiáveis.118 Portanto, mesmo em aparentemente "iguais" doses, essas diferenças podem se manifestar como diferentes respostas.
CONCLUSÕES
Os atuais estudos demonstram que as Toxinas Botulinicas exibem características biológicas e efeitos sobre muitos tipos de células humanas, o que vem aumentando as indicações de uso da mesma. Aparentemente, essas toxinas têm uma zona de influência bem maior do que o foi originalmente entendido, e esses eventos são baseados em respostas celulares individuais e os impactos colinérgicos da
BoNT - A. Os receptores da toxina botulinica e alvos intra-celulares não são únicos para a neuro-transmissão, pois vários desses receptores e alvos foram encontrados em células não neuronais.
Ainda há muito a ser aprendido sobre essas toxinas e seus mecanismos de ação. Como tal, a evidência indica que existe terreno fértil para estudos futuros, o que é altamente provável para resultar em descobertas impactantes na medicina e estética.
A nano-tecnologia vem fazendo uso do peptídeo botulinico a seu favor ,mas estudos científicos comprovando sua não sensibilização causando o efeito vacina ainda precisam ser comprovados, uma vez que o delivery do blend tópico ou via micro- agulhamento, acança a derme onde se encontram as células de Langherhans responsáveis pela resposta imunológica relacionada á pele. O intervalo de uma vez ao mes entre as três aplicações indicadas no protocolo com o micro-agulhamento, assim como o uso tópico diário por tempo prolongado podem ser passiveis que sensibilizar as células de Langherans causando o efeito vacina.
BIBLIOGRAFIA
Steinhoff, M.; Stander, S.; Seeliger, S.; Ansel, J.C.; Schmeiz, M.; Luger, T. Modern aspects of cutaneous neurogenic inflammation. Arch. Dermatol. 2003, 139, 1479– 1488.
Ansel, J.C.; Kaynard, A.H.; Armstrong, C.A.; Olerud, J.; Bunnett, N.; Payan, D. Skin-nervous system interactions. J. Investig. Dermatol. 1996, 106, 198–204.
Kellogg, D.L., Jr. In vivo mechanisms of cutaneous vasodilation and vasoconstriction in humans during thermoregulatory challenges. J. Appl. Phys. 2006, 100, 1709–1718.
Kellogg, D.L., Jr.; Pergola, P.E.; Piest, K.L.; Kosiba, W.A.; Crandall, M.; Johnson, J.M. Cutaneous active vasodilation in humans is mediated by cholinergic nerve cotransmission. Circ. Res. 1995, 77, 1222–1228.
Carmichael, M.M.; Dostrovsky, J.O.; Charlton, M.P. Peptide-mediated transdermal delivery of botulinum neurotoxin type A reduces neurogenic inflammation in the skin. Pain 2010, 149, 316–324.
Okeson, Jeffrey P., Bell”s Oral and Pacial Pain. Quitessence Publishing Co, Inc 7th ed, 2014, 46-52
Gaspar,P.K.: Neuropeptideos na pele. An.Bras.Dermatol.v.78 n.4 Rio de Janeiro jul./ago. 2003. Scielo
Bull HA, Hothersall J, Chowdhury N, Cohen J, Dowd PM.: Neuropeptides induce release of nitric oxide from human dermal microvascular endothelial cells. J Invest Dermatol 1996; 106:655-60.
Hara M, Toyoda M, Yaar M et al.: Innervation of melanocytes in human skin. J Exp Med 1996; 184:1385-95.
Schlessinger J, Gilbert E, Cohen JL, Kaufman J.Aesthet Surg J. 2017 May 1;37(suppl_1):S45-S58.
Jablonka EM, Sherris DA, Gassner HG. Botulinumtoxin to minimize facial scarring. Facial Plast Surg. 2012;28(5):525-535.
Gauglitz GG, Bureik D, Dombrowski Y, Pavicic T, RuzickaT, Schauber J. Botulinum toxin A for the treatment of keloids. Skin Pharmacol Physiol. 2012;25(6):313-318.
Xiao Z, Zhang M, Liu Y, Ren L. Botulinum toxin type ainhibits connective tissue growth factor expression in fibroblasts derived from hypertrophic scar. Aesthetic Plast Surg. 2011;35(5):802-807.
Chang CS, Wallace CG, Hsiao YC, Chang CJ, Chen PK. Botulinum toxin to improve results in cleft lip repair: a double-blinded, randomized, vehicle-controlled clinical trial. PLoS One. 2014;9(12):e115690.
Gauglitz GG. Management of keloids and hypertrophic scars: current and emerging options. Clin Cosmet Investig. Dermatol. 2013;6:103-114.
Xiao Z, Zhang F, Lin W, Zhang M, Liu Y. Effect of botulinum toxin type A on transforming growth factor beta1 in fibroblasts derived from hypertrophic scar: a preliminary report. Aesthetic Plast Surg. 2010;34(4):424-427.
Jeong HS, Lee BH, Sung HM, et al. Effect of botulinum toxin type A on differentiation of fibroblasts derived from scar tissue. Plast Reconstr Surg. 2015;136(2):171e-178e.
Ganceviciene R, Liakou AI, Theodoridis A, Makrantonaki E, Zouboulis CC. Skin anti-aging strategies. Dermatoendocrinol. 2012;4(3):308-319.
Lee SJ, Jeong SY, No YA, Park KY, Kim BJ. Combined treatment with botulinum toxin and 595-nm pulse dye laser for traumatic scarring. Ann Dermatol. 2015;27(6):756-758.
Austin, E.,Koo,E.,& Jagdeo, J.92018). The celullular Response of Keloids and Hipertrofic Scars to Botulin Toxin A. Dermatologic Surgery, 44(2), 149-157.
Roh T, Hong JW, Lee WJ, Yoon HS, et al. The effects of botulinum toxin a on collagen synthesis, expression of MMP (matrix metalloproteinases)-1,2,9 and TIMP (tissue inhibitors of metalloproteinase)-1 in the keloid fibroblasts. Arch Aesthet Plast Surg 2013;19:114–9.2013;66:439–40.
Fujiwara M, Muragaki Y, Ooshima A. Keloid-derived fibroblasts showincreased secretion of factors involved in collagen turnover and depend on matrix metalloproteinase for migration. Br J Dermatol 2005;153: 295–300.
Tanriverdi-Akhisaroglu S, Menderes A, Oktay G. Matrix metalloproteinase-2 and- 9 activities in human keloids, hypertrophic and atrophic scars: a pilot study. Cell Biochem Funct 2009;27:81–7.
Bran GM, Goessler UR, Hormann K, Riedel F, et al. Keloids: current concepts of pathogenesis (review). Int J Mol Med 2009;24:283.
´Roh T, Hong JW, Lee WJ, Yoon HS, et al. The effects of botulinum toxin a on collagen synthesis, expression of MMP (matrix metalloproteinases)-1,2,9 and TIMP (tissue inhibitors of metalloproteinase) -1 in the keloid fibroblasts. Arch Aesthet Plast Surg 2013;19:114–9.
Fujiwara M, Muragaki Y, Ooshima A. Keloid-derived fibroblasts show increased secretion of factors involved in collagen turnover and depend on matrix metalloproteinase for migration. Br J Dermatol 2005;153:295–300.
Tanriverdi-Akhisaroglu S, Menderes A, Oktay G. Matrixmetalloproteinase-2 and-9 activities in human keloids, hypertrophic and atrophic scars: a pilot study. Cell Biochem Funct 2009;27:81–7.
Bran GM, Goessler UR, Hormann K, Riedel F, et al. Keloids: current concepts of pathogenesis (review). Int J Mol Med 2009;24:283.
Failmezger C. Incidence of skin disease in Cuzco. Peru Int J Dermatol 1992;31:560–1.
Kouwenberg CA, Bijlard E, Timman R, Hovius SE, et al. Emotional quality of life is severely affected by keloid disease: pain and itch are the main determinants of burden. Plast Reconstr Surg 2015;136:150–1.
Babalola O, Mamalis A, Lev-Tov H, Jagdeo J. The role of micro RNAs in skin fibrosis. Arch Dermatol Res 2013;305:763–76.
32. Wolfram D, Tzankov A, Pülzl P, Piza-Katzer H. Hypertrophic scars and keloids— a review of their pathophysiology, risk factors, and therapeutic management. Dermatol Surg 2009;35:171–81.
33. Lee SD, Yi MH, Kim DW, Lee Y, et al. The effect of botulinum neurotoxin type A on capsule formation around silicone implants: thein vivo and in vitro study. Int Wound J 2016;13:65–71.
34. Kim S, Ahn M, Piao Y, Ha Y, et al. Effect of botulinum toxin type-a on TGF- beta/Smad pathway Signaling: implications forsilicone-induced capsule formation. Plast Reconstr Surg 2016; 138:821e–829e.
35. Jeong HS, Lee BH, Sung HM, Park SY, et al. Effect of botulinum toxin type a on differentiation of fibroblasts derived from scar tissue. Plast Reconstr Surg 2015;136:171e–178e.
Choi, J. E., Werbel, T., Wang, Z., Chi Wu, C., Yaksh, T. L., & Di Nardo, A. (2018). Botulinum toxin blocks mast cells and prevents rosacea like inflammation. Journal of Dermatological Science.doi:10.1016/j.jdermsci.2018.12.004.
Bloom BS, Payongayong L, Mourin A, Goldberg DJ. Impact of intradermal abobotulinumtoxinA on facial erythemaof rosacea. Dermatol Surg. 2015;41(Suppl 1):S9-16.
Dayan SH, Pritzker RN, Arkins JP. A new treatment regimen for rosacea: onabotulinumtoxinA. J Drugs Dermatol. 2012;11(12):e76-e79.
Park KY, Hyun MY, Jeong SY, Kim BJ, Kim MN, Hong CK. Botulinum toxin for the treatment of refractory erythema and flushing of rosacea. Dermatology. 2015;230(4):299-301.
STEINER, D. Rosácea: entenda melhor quais são os quatro subtipos desse problema de pele. São Paulo, 2016. Disponível em: http://www.minhavida.com.br
Li,Z.J.,Park,S.B.,Sonh,K.C.,Lee,Y.,Seo,Y.J.,Kim,C.C.,...Im,M.(2013).
Regulation of lipid production by acetylcholine signalling in human sebaceous glands.ournal of Dermatological Science,72(2),116-122.
Flynn TC. Advances in the use of botulinum neurotoxinsin facial esthetics. J Cosmet Dermatol. 2012;11(1):42-50.
Calvani, F., Santini, S., Bartoletti, E., & Alhadeff, A. (2018). Personal Technique of Microinfiltration With Botulin Toxin: The SINB Technique (Superficial Injection Needling Botulinum). Plastic Surgery, 229255031880033.
Aoki, K.R. Review of a Proposed Mechanism for the Antinociceptive Action of Botulinum Toxin Type A. Neurotoxicology 2005, 26, 785–793.
Cui, M.; Khanijou, S.; Rubino, J.; Aoki, K.R. Subcutaneous administration of botulinum toxin Areduces formalin-induced pain. Pain 2004, 107, 125–133.
Aoki, K.R. Review of a Proposed Mechanism for the Antinociceptive Action of Botulinum Toxin Type A. Neurotoxicology 2005, 26, 785–793.
Mense, S. Neurobiological basis for the use of botulinum toxin in pain therapy. J. Neurol. 2004,251, I1–I7.
Headache Classification Sub-committe of the International Headache Society. The International Classification of Headache Disorders 3rd edition (beta version) Cephalalgia 2013; 33(9) 629-808
Morenilla-Palao, C.; Planells-Cases, R.; Garcia-Sanz, N.; Ferrer-Montiel, A. Regulated exocytosis contributes to protein kinase C potentiation of vanilloid receptor activity. J. Biol. Chem. 2004, 279, 25665–25672.
Cheng, J.; Liu, W.; Duffney, L.J.; Yan, Z. SNARE proteins are essential in the potentiation of NMDA receptors by group II metabotropic glutamate receptors. J. Physiol. 2013, 591, 3935–3947.
Oh, H.M; Chung M.E. Botulinum Toxin for Neuropathic Pain: A Review of the Literature. Headache Classification Subcommittee of the International Headache Society (2004)The international classification of headache disorders: 2nd edition. Cephalalgia 24 (Suppl. 1): 9–160.
Matak, I.; Lackovic, Z. Botulinum toxin A, brain and pain. Prog. Neurobiol. 2014, 119–120, 39–59.
Wang, J.; Meng, J.; Lawrence, G.W.; Zurawski, T.H.; Sasse, A.; Bodeker, M.O.; Gilmore M.A.; Fernández-Salas, E.; Francis, J.; Steward, L.E.; et al. Novel chimeras of botulinum neurotoxins A and E unveil contributions from the binding, translocation, and protease domains to theirfunctional characteristics. J. Biol. Chem. 2008, 283, 1699317002.
Pal US, Kumar L, Mehta G, et al Trends in management of myofacial pain Natl J Maxillofac Surg 2014;5(2):109- 16
Wang, J.; Zurawski, T.H.; Bodeker, M.O.; Meng, J.; Boddul, S.; Aoki, K.R.; Dolly, J.O. Longer-acting and highly potent chimaeric inhibitors of excessive exocytosis created with domains from botulinum neurotoxin A and B. Biochem. J. 2012, 444, 59–67.
Alvarez D, Rockwell PG Trigger Points: Diagnosis and Management Am Fam Physician 2002;65(4):653-60
Shah JP, Thaker N, Heimur J, et al Myofascial Trigger Points Then and Now: A Historical and Scientific Perspective PM&R 2015;7(7):746-61
Wang, J.; Meng, J.; Lawrence, G.W.; Zurawski, T.H.; Sasse, A.; Bodeker, M.O.; Gilmore M.A.; Fernández-Salas, E.; Francis, J.; Steward, L.E.; et al. Novel chimeras of botulinum neurotoxins A and E unveil contributions from the binding, translocation, and protease domains to their functional characteristics. J. Biol. Chem. 2008, 283, 16993–17002
Restani, L.; Antonucci, F.; Gianfranceschi, L.; Rossi, C.; Rossetto, O.; Caleo, M. Evidence for anterograde transport and transcytosis of botulinum neurotoxin A (BoNT/A). J. Neurosci. 2011,31, 15650–15659.
60. Wang, J.; Zurawski, T.H.; Bodeker, M.O.; Meng, J.; Boddul, S.; Aoki, K.R.; Dolly, J.O. Longer-acting and highly potent chimaeric inhibitors of excessive exocytosis created with domains from botulinum neurotoxin A and B. Biochem. J. 2012, 444, 59–67.
Grando, S. A., & Zachary, C. B. (2018). The non-neuronal and nonmuscular effects of botulinum toxin: an opportunity for a deadly molecule to treat disease in the skin and beyond. British Journal of Dermatology, 178(5), 1011–1019.
Bandala C, Cort es-Algara AL, Mejia-Barradas CM et al. Botulinum neurotoxin type A inhibits synaptic vesicle 2 expression in breast cancer cell lines. Int J Clin Exp Pathol 2015; 8:8411–18
Ravichandran V, Chawla A, Roche PA. Identification of a novel syntaxin- and synaptobrevin/VAMP-binding protein, SNAP-23, expressed in non-neuronal tissues. J Biol Chem 1996; 271:13300–3.
Lee CJ, Lee MH, Cho YY. Fibroblast and epidermal growth factors utilize different signaling pathways to induce anchorage-indepen- dent cell transformation in JB6 Cl41 mouse skin epidermal cells. J Cancer Prev 2014; 19:199–208.
I X, Coffield JA. Structural and functional interactions between transient receptor potential vanilloid subfamily 1 and botulinum neurotoxin serotype A. PLOS ONE 2016; 11:e0143024.
Park JR, Lee H, Kim CH et al. Functional characteristics of mes- enchymal stem cells derived from the adipose tissue of a patient with achondroplasia. In Vitro Cell Dev Biol Anim 2016; 52:545–54.
Zhu Z, Stone HF, Thach TQ et al. A novel botulinum neurotoxin topical gel: treatment of allergic rhinitis in rats and comparative safety profile. Am J Rhinol Allergy 2012; 26:450–4.
Anna-Mitchell AT, Wolf-Johnston AS, Barrick SR et al. Effect of botu- linum toxin A on urothelial-release of ATP and expression of SNARE targets within the urothelium. Neurourol Urodyn 2015; 34:79–84.
Couesnon A, Shimizu T, Popoff MR. Differential entry of botuli- num neurotoxin A into neuronal and intestinal cells. Cell Microbiol 2009; 11:289–308.
Kitas GD, Salmon M, Emery P. Immune dysfunction in patients not responding to hepatitis B vaccination. Lancet 1989; 1:551–2.
Proietti S, Nardicchi V, Porena M, Giannantoni A. [Botulinum toxin type-A toxin activity on prostate cancer cell lines]. Urologia 2012; 79:135–41.
Zimmerman UJ, Malek SK, Liu L, Li HL. Proteolysis of synapto- brevin, syntaxin, and SNAP-25 in alveolar epithelial type II cells. IUBMB Life 1999; 48:453–8.
Nabokina S, Egea G, Blasi J, Mollinedo F. Intracellular location of SNAP-25 in human neutrophils. Biochem Biophys Res Commun 1997; 239:592–7.
Kim YJ, Kim JH, Lee KJ et al.Botulinum neurotoxin type A induces TLR mediated inflammatory responses in macrophages. PLOS ONE 2015; 10:e0120840.
Sugawara Y, Yutani M, Amatsu S et al. Functional dissection of the Clostridium botulinum type B hemagglutinin complex: identification of the carbohydrate and E- cadherin binding sites. PLOS ONE 2014; 9: e111170.
Sugawara Y, Iwamori M, Matsumura T et al. Clostridium botulinum type C hemagglutinin affects the morphology and viability of cultured mammalian cells via binding to the ganglioside GM3. FEBS J 2015; 282:3334–47.
Thirunavukkarasusx N, Ghosal KJ, Kukreja R et al. Microarray analysis of differentially regulated genes in human neuronal and epithelial cell lines upon exposure to type A botulinum neuro- toxin. Biochem Biophys Res Commun 2011; 405:684–90.
Karsenty G, Rocha J, Chevalier S et al. Botulinum toxin type A inhibits the growth of LNCaP humanprostate cancer cells in vitro andin vivo. Prostate 2009; 69:1143–50.
Esca SA, Holub G, Pimpl W. [Wegener’s granulomatosis]. Hautarzt 1984; 35:379–82.
Nishiyama Y, Yokoyama T, Tomizawa K et al. Effects of purifiednewly developed botulinum neurotoxin type A in rat prostate. Urology 2009; 74:436–9.
Gorgal T, Charrua A, Silva JF et al. Expression of apoptosis-regulating genes in the rat prostate following botulinum toxin type A injection. BMC Urol 2012; 12:1.
Batifol, D., Huart, A., Finiels, P. J., Nagot, N., & Jammet, P. (2018). Effect of intra-articular Botulinum toxin injections on temporo-mandibular joint pain. Journal of Stomatology, Oral and Maxillofacial Surgery. doi:10.1016/j.jormas.2018.06.002
Aoki, Kr. Review of a proposed mechanism for the antinociceptive action of botulin toxin type A. Neurotoxicology 2005; 26:785-93.
Cui M, Khanijoi S, Rubino J, Aoki, KR. Subcutaneous administration of botulin toxin A reduces formalina-induced pain. Pain 2004; 107:125-33
Birklein F. ,Schmelz, M. Neuropeptides, neurogenic imflamation and complex regional pain syndrome ( CRPS). Neurosci. Lett. 20008; 437:199-202.
Aoki KR, Francis J. Updates on the antinociceptive mechanism hypothesis of botulim toxin A. Parkisonism Relat Disor. 2011; 17:S28-29.
Pavicic T, Few W.J, Feew, Vorländer J. H. A Novel, Multistep, Combination Facial Rejuvenation Procedure for Treatment of the Whole Face With Incobotulinumtoxin A, and Two Dermal Fillers - Calcium Hydroxylapatite and a Monophasic, PolydensiFed Hyaluronic Acid. September 2013 | Volume 12 | Issue 9 | Original Article | 978 | Copyright © September 2013.
Schlessinger J, Gilbert E, Cohen JL, Kaufman J. Aesthet Surg J. 2017 May 1;37(suppl_1):S45-S58. Review.
Ascher B, Fanchon C, Kanoun-Copy L, Bouloc A, Benech. A skin care containing retinol adenosine and hyaluronicacid optimises the benefits from a type A botulinum toxin injection. J Cosmet Laser Ther. 2012;14(5):234-238.
Beer KR, Julius H, Dunn M, Wilson F. Remodeling of periorbital, temporal, glabellar, and crow’s feet areas with hyaluronic acid and botulinum toxin. J Cosmet Dermatol.2014;13(2):143-150.
Lorenc ZP, Daro-Kaftan E. Optimizing facial rejuvenation outcomes by combining poly-L-lactic acid, hyaluronicacid, calcium hydroxylapatite, and neurotoxins: two case studies. J Drugs Dermatol. 2014;13(2):191-195.
Molina B, David M, Jain R, et al. Patient satisfaction and efficacy of full-facial rejuvenation using a combinationof botulinum toxin type A and hyaluronic acid filler. Dermatol Surg. 2015;41(Suppl 1):S325-S332.
Rubin MG, Cox SE, Kaminer MS, Solish N. Correctingage-related changes in the face by use of injectable fillers and neurotoxins. Semin Cutan Med Surg. 014;33
(4 Suppl):S81-S84.Schlessinger J, Kenkel J, Werschler P. Further enhancement of facial appearance with a hydroquinone skin caresystem plus tretinoin in patients previously treated with botulinum toxin Type A. Aesthet Surg J. 2011;31(5):529-539.
Schlessinger J, Erin Gilbert, Cohen J.L, Kaufman J. New usue of Abobotulinium toxin- A in Cosmetics. . Aesthet Surg J.2017;37(S1) S45-S48.
Dubina M, Tung R, Bolotin D, et al. Treatment of forehead/glabellar rhytide complex with combination botulinum toxin a and hyaluronic acid versus botulinum toxin-A injection alone: a split-face, rater-blinded, randomized control trial. J Cosmet Dermatol. 2013;12(4):261-266.
Wu WTL. Microbotox of the lower face and neck: evolution of a personal technique and its clinical effects. PlastReconstr Surg. 2015;136(5 suppl):92S-100S.
JongSeo Kim, Clinical Effects on Skin Texture and Hydration of the Face Using Microbotox and Microhyaluronicacid PRS Global Open. 2018.
Ganceviciene R, Liakou AI, Theodoridis A, Makrantonaki E, Zouboulis CC. Skin anti-aging strategies. Dermatoendocrinol. 2012;4(3):308-319.
Permatasari F, Hu YY, Zhang JA, Zhou BR, Luo D.Anti-photoaging potential of Botulinum toxin type A in UVB-induced premature senescence of human dermal fibroblasts in vitro through decreasing senescence-related proteins. J Photochem Photobiol B. 2014;133:115-123.
Carruthers J, Carruthers A. The effect of full-face broadband light treatments alone and in combination with bilateral crow’s feet Botulinum toxin type A chemo- denervation. Dermatol Surg. 2004;30(3):355-366;discussion 366.
Môle B. Accordion wrinkle treatment through the targeted use of botulinum toxin injections. Aesthetic Plast Surg. 2014;38(2):419-428.
Môle B. Griffose faciale: traitement des rides dynamiques du visage par inject- tions dermiques simultanées de toxine botulique A et d’acide hyaluronique. Ann Chir Plast Esthet. 2012;57(3):194-201.
Pavicic T, Gauglitz GG, Lersch P, et al. Efficacy of cream based novel formulations of hyaluronic acid of differentmolecular weights in anti-wrinkle treatment. J Drugs Dermatol. 2011;10(9):990-1000.
Môle B. Accordion wrinkle treatment through the targeted use of botulinum toxin injections. Aesthetic Plast Surg. 2014;38(2):419-428.
Môle B. Griffose faciale: traitement des rides dynamiquesdu visage par injections dermiques simultanées de toxine botulique A et d’acide hyaluronique. Ann Chir Plast Esthet. 2012;57(3):194-201.
Yamauchi PS, Lask G, Lowe NJ. Botulinum toxin type-A gives adjunctive benefit to periorbital laser resurfacing. J Cosmet Laser Ther. 2004;6(3):145-148.
Khoury JG, Saluja R, Goldman MP. The effect of botulinum toxin type A on full- face intense pulsed light treatment: a randomized, double-blind, split-face study. Dermatol Surg. 2008;34(8):1062-1069.
Pavicic T, Gauglitz GG, Lersch P, et al. Efficacy of cream based novel formu- lations of hyaluronic acid of different molecular weights in anti-wrinkle treatment. J Drugs Dermatol. 2011;10(9):990-1000.
Mahmoud BH, Burnett C, Ozog D. Prospective randomizedcontrolled study to determine the effect of topical application of botulinum toxin A for crow’s feet after treatment with ablative fractional CO2 laser. Dermatol Surg. 2015;41(Suppl 1):S75- S81.
Abella ML. Evaluation of anti-wrinkle efficacy of adenosine-containing products using the FOITS technique. Int J Cosmet Sci. 2006;28(6):447-451.
Ascher,B.,Fanchon,C., Kanoun-copy, L.,Bouloc, A.,& Benech, F. (2012). A skincare containing retinol adenosine and hyaluronic acid potimises the benefits from a type A toxin injection. Journal of Cosmetic and Laser Therapy, 14(5), 234-238.
Abella ML . E valuation of anti-wrinkle efficacy of adenosine containing product using the FOITS technique . Int. J. Cosmetic Science . 2006 ; 28 : 447 – 451 .
Botulinum tópico é apresentado pela Meiskin Swiss. 115. S.Meiskin.
Valença, João Luis- Microagulhamento com peptídeo botulínico, a evolução em ativos nano. Live da Abrahof em 22/04/2020 pelo Instagran.
Kim JE, Song EJ, Choi GS, Lew BL, Sim WY, Kang H. The efficacy and safety of liquid-type botulinum toxin type A for the management of moderate to severe glabellar frown lines. Plast Reconstr Surg. 2015;135(3):732-741.
Carruthers J, Fournier N, Kerscher M, Ruiz-Avila J,Trindade de Almeida AR, Kaeuper G. The convergenceof medicine and neurotoxins: a focus on botulinum toxin type A and its application in aesthetic medicine-a global,evidence-based botulinum toxin consensus education initiative: part II: incorporating botulinum toxin into aesthetic clinical practice. Dermatol Surg. 2013;39(3 Pt 2):510-525.
Oliveira G.B., Rossi N.C.P, Moreira B.M.T- Tratamento da porção inferior do músculo orbicular dos olhos com microdoses de toxina botulinica: série de 300 casos. Surg Cosmet Dermatol 2016;8(3):206-9.
Linha Meiskin Swiss com Peptideo Botulínico em nanotecnologia para uso tópico.
Disponível em: https://panoramafarmaceutico.com.br/2019/09/17/b. Acesso em 23/05/20. Monografia Meiskin Swiss, disponível com o próprio fabricante.
Glogau R, Blitzer A, Brandt F, Kane M, Monheit GD,Waugh JM. Results of a randomized, double-blind, placebo-controlled study to evaluate the efficacy and safety of a botulinum toxin type A topical gel for the treatment of moderate-to-severe lateral canthal lines. J Drugs Dermatol.2012;11(1):38-45.
Mahmoud BH, Ozog D, Burnett C, Cohen JL. Prospective randomized split-face comparative study between topical botulinum toxin A surface application and local injection for Crow’s feet. Dermatol Surg. 2016;42(4):554-556.
Zhu J, Ji X, Li M, et al. The efficacy and safety of fractional CO2 laser combined with topical type A botulinum toxin for facial rejuvenation: a randomized controlled split-face study. Biomed Res Int. 2016;2016:3853754.
Mahmoud BH, Burnett C, Ozog D. Prospective randomized controlled study to determine the effect of topical application of botulinum toxin A for crow’s feet after treatment with ablative fractional CO2 laser. Dermatol Surg. 2015;41(Suppl 1):S75- S81.
Revance Therapeutics. Revance Reports Results forRT001 Topical Phase 3 Trial for Lateral Canthal Lines.GlobeNewswire News Room. 2016. Available from: https://globenewswire.com/news-release/2016/06/13/848193/0/en/Revance-Reports- Results -for-RT001-Topical-Phase-3- Trial-for-Lateral-Canthal-Lines.html. Accessed 25 July 2016.
Download