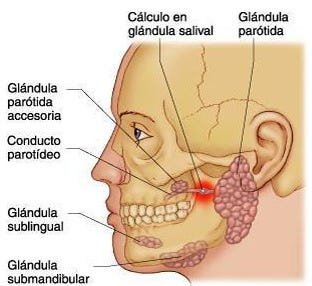
Você já ouviu falar de alguém que começa a suar no rosto, especialmente na região das bochechas e têmporas, simplesmente ao comer ou até mesmo ao pensar em comida? Esse sintoma peculiar, conhecido como sudorese gustativa, é a principal característica da Síndrome de Frey. Embora não seja uma condição grave, o impacto social e emocional pode ser significativo, afetando a qualidade de vida e a autoconfiança de quem convive com ela.
Frequentemente associada a cirurgias na glândula parótida, essa síndrome tem um tratamento que se destaca pela sua eficácia e simplicidade: a aplicação de toxina botulínica. Como exatamente essa substância, famosa por tratar rugas, atua nesse caso?
Para explorar o tema, apresentamos uma adaptação do trabalho de conclusão de curso de Bianca Bená Theodoro, realizado para a obtenção do título de Especialista em Harmonização Orofacial pelo Instituto Velasco. Continue a leitura para entender as causas, o diagnóstico e como a toxina botulínica se tornou o tratamento de eleição para a Síndrome de Frey.
A Síndrome de Frey, também conhecida por Sudorese Gustativa ou Síndrome Auriculotemporal, é caracterizada por suor, calor e hiperemia na face, principalmente nas regiões parótidas e malares, durante a mastigação. Embora a síndrome não provoque nenhuma doença física, ela causa desconforto emocional e psicológico, tanto no meio pessoal quanto no social, uma vez que desencadeia uma espécie de fobia. Esta fobia faz com que o paciente viva preocupado com o prejulgamento dos outros, já que a síndrome se manifesta por meio da transpiração na face durante a refeição ou a estimulação salivar, especialmente ao ingerir alimentos com sabores mais intensos, como os alimentos ácidos, condimentados ou salgados, sem que ele tenha nenhum controle sobre isso. A síndrome também pode desencadear sintomas na distribuição do nervo auricular maior, havendo rubor e calor em excesso na região da bochecha (1).
Na literatura, a Síndrome de Frey é descrita como uma complicação após a parotidectomia e é precipitada por qualquer tipo de estímulo gustatório. Os sintomas geralmente surgem seis meses após o procedimento cirúrgico, tempo necessário para a regeneração do nervo lesado, mas podem apresentar-se tardiamente, como no caso pesquisado em que os sintomas apareceram 20 anos após a cirurgia (2).
O primeiro caso da síndrome foi descrito pelo Dr. Baillarger em 1853, após a drenagem de um abscesso parotídeo. Apesar de a patofisiologia estar incorreta, pois ele relacionava a sudorese com o bloqueio do ducto de Stenon, foi a Dra. Lucie Frey que, em 1923, descreveu os sintomas de forma correta e deu a perspectiva adequada sobre a relevância da inervação autonômica da glândula parótida e da pele. Por isso, em reconhecimento, a síndrome leva seu nome. Ao apontar com precisão a função do nervo auriculotemporal na síndrome, Frey forneceu a conexão ausente entre a estimulação alimentar e gustatória de um lado e a produção de sudorese facial do outro (3).
Atualmente, aceita-se a teoria da regeneração aberrante, na qual fibras parassimpáticas do nervo auriculotemporal são lesadas durante a cirurgia e, no processo de regeneração, estas fibras juntam-se às fibras simpáticas das glândulas sudoríparas subcutâneas. Assim, o reflexo salivar que ocorre durante a mastigação, além de induzir a produção de saliva, também vai induzir a sudorese e o eritema da região parótida (4).
Objetivo
O objetivo deste trabalho foi verificar a tese da eficácia da aplicação da Toxina Botulínica tipo A em pacientes que foram submetidos à parotidectomia e tiveram a confirmação da Síndrome de Frey após o teste de Minor do iodo e amido. Além disso, busca constatar, por meio de estudos, se a aplicação da Toxina Botulínica tipo A é um tratamento viável, menos invasivo e se há efeitos colaterais, conseguindo assim proporcionar aos pacientes uma melhor qualidade de vida.
Revisão Literária
História da Doença
A hiperidrose (produção de suor acima da quantidade considerada normal) ocorre tanto no frio quanto no calor, em situações de ansiedade, nervosismo ou não, realizando atividades ou não; ou seja, independe de uma situação externa (1). Sua origem é desconhecida e ela pode se manifestar nas regiões craniofacial, axilar, plantar ou palmar e, ocasionalmente, afeta regiões simultaneamente (5).
Tillman et al. (6) em 2014 esclareceram os trabalhos da neurologista polonesa Dra. Lucie Frey, que identificou o papel do sistema auriculotemporal. O nervo auriculotemporal é um ramo da divisão mandibular do nervo trigêmeo. Ele sai do crânio através do forame oval, vira superiormente, anterior ao auditivo externo e paralelo ao temporal superficial, que inerva os vasos do couro cabeludo.
O mecanismo mais amplamente aceito para o desenvolvimento da Síndrome de Frey resulta da reinervação de glândulas sudoríparas colinérgicas e vasos na pele com fibras parassimpáticas pós-ganglionares do nervo auditivo temporal que foram expostas ou feridas, ou seja, é uma regeneração nervosa mal direcionada (7).
A lesão no nervo auriculotemporal resultante de parotidectomia ou trauma na região da parótida pode prejudicar o estado parassimpático das fibras simpáticas e da glândula parótida. No processo de regeneração nervosa, fibras parassimpáticas podem emergir como uma conexão errada e crescer junto com as extremidades cortadas das fibras simpáticas para as glândulas sudoríparas e vasos sanguíneos da pele. A regeneração supõe que as fibras parassimpáticas que normalmente inervam a glândula parótida, depois de perderem seus alvos durante a parotidectomia, regeneram-se para inervar os vasos da pele facial e as glândulas sudoríparas. A função normal dessas fibras é aumentar a secreção salivar durante a alimentação, e sua ativação após a regeneração estimula os novos alvos durante as refeições, resultando em vasodilatação local (rubor gustativo) и sudorese gustativa (4).
Para que o processo de regeneração ocorra, as fibras simpáticas do tecido cutâneo facial e as glândulas sudoríparas devem ser danificadas. Este é um evento que ocorre após a cirurgia da parótida ou um trauma penetrante na região (4).
Diagnóstico
O diagnóstico baseia-se no relato do paciente e nas condições clínicas após ele se alimentar, tendo o histórico de parotidectomia ou trauma na região da parótida.
Tratamento
Embora a Síndrome de Frey seja provavelmente um efeito colateral inevitável da parotidectomia, apenas cerca de metade dos pacientes é sintomática. Entre estes, cerca de metade julga seus sintomas como importantes ou embaraçosos. Para esses pacientes, diferentes tratamentos foram tentados com sucesso limitado.
Dulguerov et al. (4) em 1997 classificaram os tratamentos nos seguintes grupos:
Seção de alguma parte do arco eferente (neurectomia timpânica);
Radioterapia;
Anticolinérgico tópico local;
Reoperação e colocação de uma interposição de barreira.
Beerens et al. (9) em 2001 descreveram o tratamento em pacientes com queixas graves utilizando Toxina Botulínica tipo A. Foi realizado o teste de Minor (iodo e amido) para comprovar a transpiração. A área afetada foi dividida em quadrantes de 4 cm², e foi aplicado Dysport (7,5 unidades por ponto). Constatou-se que a recidiva dependia do tamanho da área afetada: quanto menor a área, mais tempo durava o efeito da toxina.
Jansen et al. (10) em 2017 trataram 440 pacientes e utilizaram três tipos de toxina: Botox, Dysport e Xeomin. O Botox e o Xeomin mostraram-se mais precisos na dosagem, com efeito duradouro e estável.
Muraro et al. (1) em 2019 utilizaram Toxina Botulínica tipo A no tratamento da hiperidrose, com melhora significativa na qualidade de vida dos pacientes.
Díaz et al. (11) em 2007 aplicaram 38 unidades de Toxina Botulínica tipo A, observando melhora a partir do quinto dia e meio após a aplicação. Foi necessária uma segunda dose, em média, 18 meses após a primeira.
Pavelecini et al. (12) em 2003 deram ênfase a técnicas profiláticas, como a interposição de uma barreira mecânica (materiais sintéticos, enxertos, retalhos) entre o leito parotídeo e a pele.
Shah et al. (13) em 2017 estudaram a Síndrome de Frey pós-herpética, cujo tratamento varia de aplicação tópica de glicopirrolato a injeções locais de toxina e intervenções cirúrgicas.
Bree et al. (14) em 1999 administraram injeções repetidas de Dysport, mostrando uma diminuição do tamanho da área afetada e um aumento na duração dos efeitos da toxina.
Lessa et al. (15) em 2010 trataram a fobia social associada à hiperidrose com Toxina Botulínica tipo A, combinada com terapia cognitivo-comportamental, proporcionando alívio dos sintomas.
Freni et al. (2) trataram um paciente cujos sintomas apareceram 20 anos após a parotidectomia. Os sintomas retornaram 25 meses após a primeira aplicação da toxina. Após 3 anos da segunda dosagem, ainda não havia sinais de retorno da síndrome.
Na literatura, existem onze tipos de tratamento descritos, mas a maioria é ineficiente a longo prazo ou possui efeitos colaterais piores que os sintomas. A técnica mais eficiente, menos invasiva e sem danos colaterais para o tratamento da Síndrome de Frey é a aplicação de Toxina Botulínica tipo A.
A Toxina Botulínica
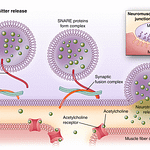
Na natureza, as neurotoxinas botulínicas são sintetizadas como parte de um complexo molecular (16). Essa neurotoxina entra no citoplasma de células nervosas periféricas e decompõe a proteína SNAP-25, essencial para a exocitose da acetilcolina. Dessa forma, a neurotransmissão é bloqueada até que a reinervação ocorra (9).
Muraro et al. (1) afirmam que o mecanismo de ação da BTX-A é a clivagem da proteína de membrana SNAP-25. Assim, a acetilcolina (ACh) permanece nas vesículas, inibindo o estímulo para a produção de suor. O processo ocorre em etapas: a toxina se liga ao terminal nervoso, é internalizada, e sua cadeia leve cliva a enzima SNAP-25, impedindo a liberação de ACh. O efeito é temporário e reversível, pois novos brotos axonais se formam, restabelecendo a atividade. Atualmente, existem três fórmulas de toxina tipo A: Botox (ONBoNT), Xeomin (INBoNT) e Dysport (ABoNT) (10).
A Toxina Botulínica é contraindicada em gestantes, lactantes e em casos de doenças neuromusculares ou alergias aos componentes (17). Nigam et al. (18) em 2010 descreveram que sua aplicação é considerada segura, com poucas complicações.
Toxina Botulínica no Tratamento da Síndrome de Frey
A Toxina Botulínica atua como um anticolinérgico, sendo eficaz porque as sinapses parassimpáticas regeneradas são colinérgicas, ao contrário de outras sinapses simpáticas (4). A presença de um neurotransmissor idêntico entre a inervação normal e a regenerada é um requisito para a regeneração aberrante (4). Em 1994, a injeção de Toxina Botulínica tipo A demonstrou eficácia ao reduzir a sudorese sem efeitos colaterais graves (7).
A Síndrome de Frey em Crianças
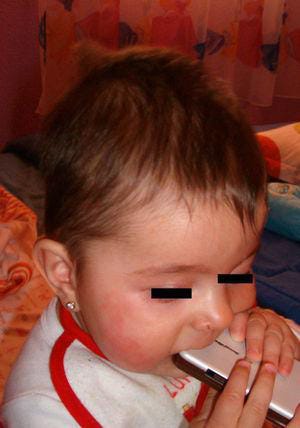
A síndrome de Frey em crianças é rara e frequentemente atribuída erroneamente à alergia alimentar. Na realidade, resulta de trauma perinatal, onde o nervo auriculotemporal é lesionado por fórceps no momento do nascimento (6). Os autores relatam casos de eritema facial unilateral em crianças após a ingestão de alimentos, como banana, sem outros sintomas associados (6).
Em crianças, muitas vezes há apenas a presença de rubor gustativo, sem suor, o que é chamado de Síndrome de Frey incompleta ou atípica (6). Embora a injeção intradérmica de toxina possa ser considerada, nenhum tratamento para essa condição benigna em crianças se faz necessário (6).
Casos Clínicos
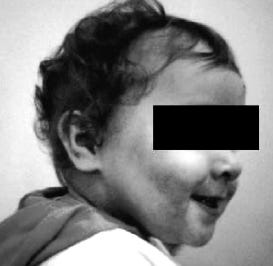
Paciente Criança
Menina de 6 meses de idade com eritema e leve edema na bochecha direita após a introdução de frutas na alimentação. No período neonatal, a paciente apresentou grande lesão na bochecha direita, secundária a trauma obstétrico por fórceps (6).
Paciente do Sexo Feminino
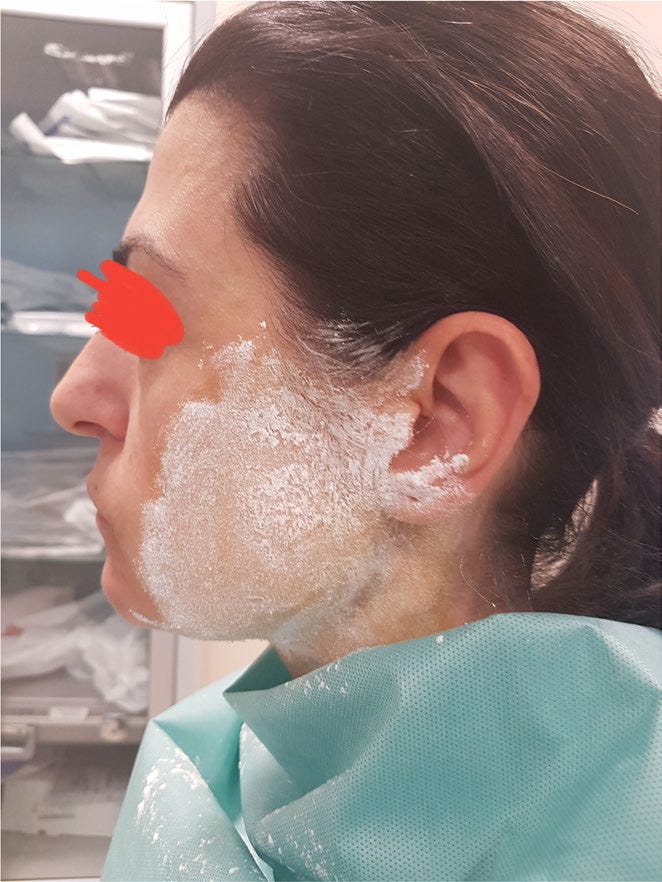
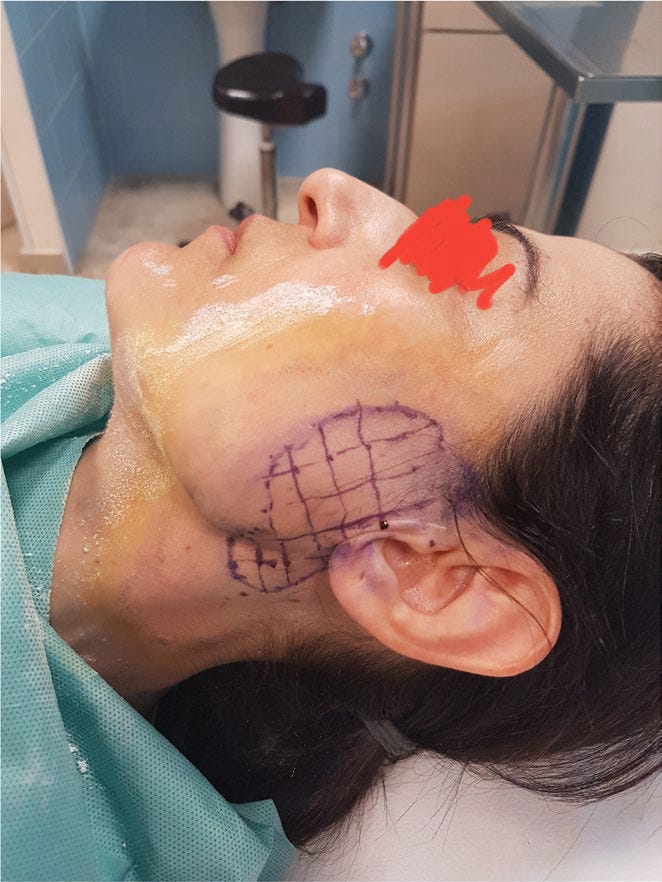
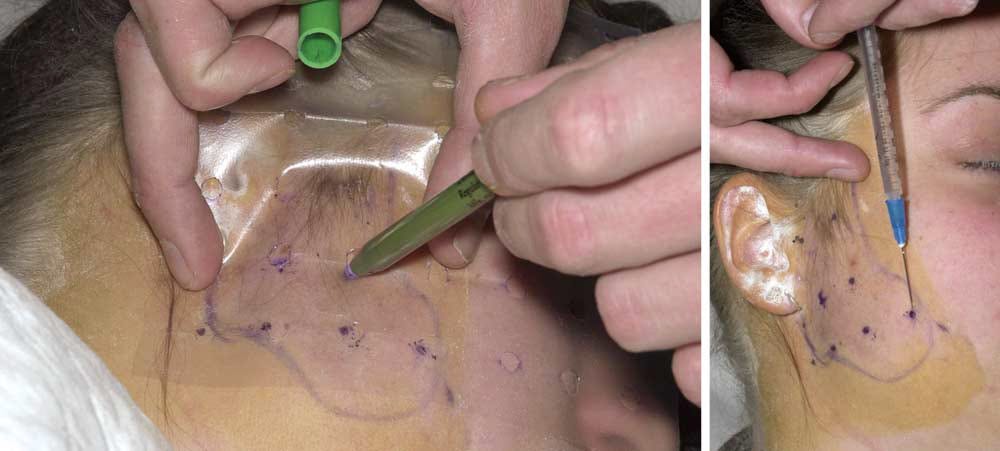
Paciente de 42 anos, operada há 20 anos de parotidectomia bilateral. Foi diagnosticada com Síndrome de Frey por meio do teste de Minor. Após aplicação de solução de iodo e pó de amido, a área ficou marrom-violeta. A área foi dividida em quadrados de 1 cm² e tratada com Toxina Botulínica. A paciente só voltou a ter sintomas 25 meses depois, quando repetiu o tratamento (2).
[IMAGEM AQUI]
Legenda
Paciente do Sexo Masculino
Paciente de 64 anos, com Diabetes Mellitus, queixou-se de hipersudorese da face, pescoço e couro cabeludo durante as refeições. O envolvimento de uma área extensa e a preferência por um tratamento mais cômodo levaram à instituição de terapêutica oral com oxibutinina, que proporcionou alívio imediato (21).
Método
Foram pesquisadas as bases de dados PubMed, Bireme e Google Scholar com as palavras-chave “Frey’s Syndrome”, “auriculotemporal syndrome”, “Botulinum Toxin”, “gustatory sweating”, “Hyperhidrosis” e “Parotid Gland”. Foram selecionados 42 artigos e utilizados 27, excluindo-se aqueles que não apresentaram análises de exames, entrevistas ou registros fotográficos na literatura.
Métodos de Tratamento
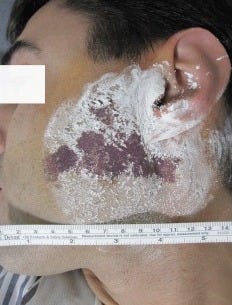
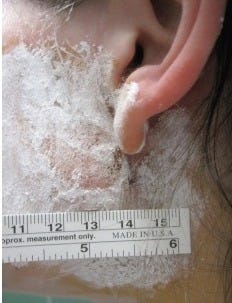
O teste de Minor consiste em tingir a pele das regiões parótidas e zigomática com iodo a 3% em solução de etanol. Após secar, polvilha-se amido no local e oferece-se um alimento ao paciente. A presença de sudorese e a reação de coloração (azul escuro) confirmam a Síndrome de Frey (9). A área colorida é marcada, medida e dividida em quadrados para indicar os locais onde a toxina botulínica deve ser aplicada (9).
A toxina utilizada foi o Dysport. Uma ampola de 500 unidades foi dissolvida em 6,67 ml de cloreto de sódio a 0,9%, resultando em uma concentração de 75 unidades/ml. Cerca de 0,1 ml corresponde a 7,5 unidades injetadas intracutaneamente por 4 cm².
Em outro estudo, em Colônia, 440 pacientes foram testados. A área afetada foi subdividida em quadrados de 1 cm², e foram injetadas unidades de Botox, Xeomin ou Dysport (10).
Em Madrid, 10 pacientes foram selecionados e, após aplicação de uma folha de celulose com iodo, a área de sudorese foi medida. Em todos os casos, foi registrado se o SMAS (sistema musculoaponeurótico superficial) havia sido danificado (11).
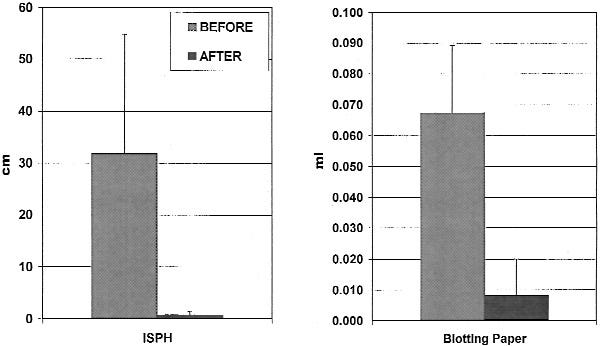
Em Genebra, 12 pacientes foram analisados. A quantidade e a superfície do suor foram medidas com papel blotting e papel sublimado com iodo. Após mapear a área, a Toxina Botulínica (5 U por 0,1 ml) foi injetada por via intradérmica (4).
De acordo com os pesquisadores de Amsterdã, a maioria dos pacientes teve uma diminuição de mais de 90% da sudorese gustativa após 3 meses. A recorrência ocorreu, em média, após 11 meses (9).
Discussão
A realização de parotidectomia parcial, em vez da completa, sempre que o tumor permitir, reduzirá a incidência da Síndrome de Frey (9). Diversos fatores, como a técnica cirúrgica e os métodos de avaliação, influenciam a incidência da síndrome (4).
A Síndrome de Frey pode ser classificada como moderada ou grave, e seus sintomas podem ser precipitados por qualquer tipo de alimento, incluindo rubor, suor e eritema (13). O teste mais utilizado para avaliar a sudorese gustativa é o do iodo e amido (13).
O tratamento apenas se justifica se interferir nas atividades diárias do paciente ou causar embaraço social (23). Ele inclui medicamentos (anticolinérgicos) e medidas cirúrgicas. As injeções intracutâneas de Toxina Botulínica tipo A são uma opção de tratamento médico (13).
A teoria da regeneração aberrante supõe que as fibras parassimpáticas, que normalmente inervam a glândula parótida, regeneram-se para inervar os vasos da pele e as glândulas sudoríparas, resultando em vasodilatação (rubor gustativo) e sudorese localizada (4).
A eficácia e a segurança da Toxina Botulínica tipo A no tratamento foram evidenciadas em 22 artigos. A injeção de toxina mostrou-se eficaz em reduzir ou abolir o efeito da sudorese (7).
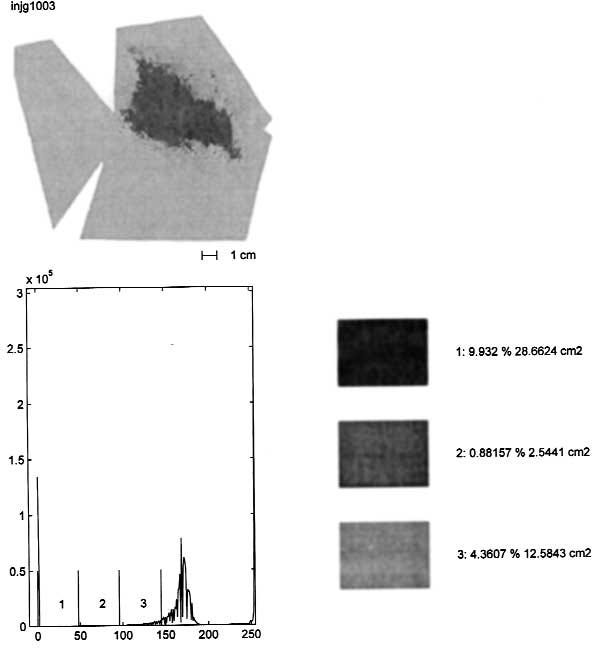
[IMAGEM AQUI]
Legenda Figura 11: A impressão do estêncil digitalizada é mostrada no histograma (4).
Dr. Lindern e sua equipe trataram pacientes com Toxina Botulínica tipo A, e os sintomas desapareceram completamente, sem necessidade de uma segunda aplicação no período de 23 meses (3).
Considerações Finais
Após todas as análises, conclui-se que o tratamento é necessário para os pacientes que se queixam de grande incômodo após a parotidectomia. O método utilizado para a constatação da síndrome foi o teste de Minor do iodo e amido.
Apesar de vários tratamentos terem sido propostos, o mais adequado e com melhora visível é a aplicação por via intradérmica da Toxina Botulínica tipo A na área afetada. O tratamento se mostrou simples, eficaz, confiável, rápido e sem efeitos colaterais aparentes.
Após a aplicação da toxina, todos apresentaram uma redução significativa da sudorese. O tratamento repetido diminui cada vez mais os sintomas, o tamanho da área afetada e prolonga a duração do efeito, pois a capacidade regenerativa dos nervos simpáticos provavelmente se torna limitada.
Conclusão
Embora a Síndrome de Frey seja um efeito posterior inevitável da parotidectomia, apenas cerca de metade dos pacientes é sintomática. Vários métodos foram utilizados para tratar a síndrome, com diferentes graus de eficácia, dividindo-se em cirúrgicos e não invasivos. De todos os métodos propostos, o que se mostrou mais assertivo e menos invasivo no tratamento da síndrome é a Toxina Botulínica tipo A.
Fontes, Referências e Bibliografia
Murato CSP, Marques SA, Rocha-Lima ABC, Oliveira DAG, Lopes ES, Aparecido CTR, et al. Botulinum Toxin Type A in the Treatment of Hyperhidrosis: Case Study. Jundiaí; 2019.
Freni F, Gazia F, D’Alcontres FS, Galletti B, Galletti F. Use of botulinum toxin in Frey’s syndrome. Messina; 2018.
Lindern JJV, Niederhagen B, Bergé S, Hägler G, Reich RH. Frey Syndrome Treatment with Type A Botulinum Toxin. Bonn; 2000.
Dulguerov P, Quinodoz D, Cosendai G, Piletta P, Lehmann W. Frey syndrome treatment with botulinum toxin. Genebra; 1997.
Resina E, Jones-Caballero M, Hernández-Núñez A, Pascual M, Tello ED. Hiperhidrosis localizada. Evaluación de la efectividad, calidad de vida, seguridad y satisfacción tras el tratamiento con toxina botulínica. Madrid; 2017.
Tillman BN, Lesperance MM, Brinkmeier JV. Infantile Frey’s syndrome. Int J Pediatr Otorhinolaryngol. 2014;78(7):1135-7.
Xie S, Wang K, Xu T, Guo XS, Sham XF, Cai ZG. Efficacy and safety of botulinum toxin type A for treatment of Frey’s syndrome: evidence from 22 published articles. Pequim; 2015.
Glândulas Salivares – Funcionamento e o que são [Internet]. umCOMO; 2018 [citado 5 jan 2020]. Disponível em: https://educacao.umcomo.com.br/artigo/glandulas-salivares-funcionamento-e-o-que-sao-3294.html
Beerens AJF, Snow GB. Botulinum toxin A in the treatment of patients with Frey syndrome. Amsterdã; 2001.
Jansen S, Jerowski M, Ludwig L, Fischer-Krall E, Beuetner D, Grosheva M. Botulinum toxin therapy in Frey’s syndrome: a retrospective study of 440 treatments in 100 patients. Cologne; 2017.
Díaz PM, Castilho RB del, Prata MM, Gias LN, Nieto GM, Lee GYC, et al. Clinical results in the management of Frey’s Syndrome with injections of Botulinum Toxin. Madrid; 2007.
Pavelecini M, Valente DS, Borile G, Fontana C, Webster R, Chem RC. O retalho de Smas na profilaxia da síndrome de Frey em parotidectomias. Blumenau; 2003.
Shah JS, Asrani VK. Post Herpetic Frey’s Syndrome. Gujarat; 2017.
Bree R, Duyndam J, Kuik DJ, Leemans CR. Use of botulinum toxin in Frey’s syndrome. Amsterdã; 1999.
Lessa LR, Fontenelle LF. Toxina botulínica como tratamento para fobia social generalizada com hiperidrose. Rio de Janeiro; 2010.
Aoki KR. Pharmacology of Botulinum neurotoxins. Oper Tech Otolaryngol Head Neck Surg. 2004;15(2):85-9.
Klein AW. Contraindications and complications with the use of botulinum toxin. 2004.
Nigam PK, Nigam A. Botulinum toxin. Indian J Dermatol. 2010;55(1):8-14.
Mozes F, Tukiyama FU, Castro APBM, Corradi GA, Pastorino AC, Fomin ABF, et al. Síndrome de Frey simulando eritema malar por alergia alimentar. Rev Paul Pediatr. 2007;25(4):387-90.
Baylach J, Martinez A, Aragó T, Galdós H, Herrera C, Abajo IR. Síndrome de Frey secundário a traumatismo obstétrico. An Pediatr (Barc). 2009;71(4):353-5.
Gill F, Figueiredo A, Dias M, Aranha J, Esteves MC. Hiperidrose Gustativa na Diabetes Mellitus – A propósito de um caso clínico. Santarém; 2017.
Goulart A, Soares V, Koch P. Prevalência de Síndrome de Frey após Parotidectomia. Lisboa; 2013.
Lopes T, Barroso L, Mesquita M, Bitoque S, Lopez D, Ferreira A. Síndrome de Frey – Uma visão global do tema. Rev Port Estomatol Med Dent Cir Maxilofac. 2012;53(4):236-42.
Downloads